

高等学校化学学报 ›› 2018, Vol. 39 ›› Issue (7): 1406.doi: 10.7503/cjcu20170261
收稿日期:2018-03-12
出版日期:2018-07-10
发布日期:2018-06-21
作者简介:联系人简介: 徐家宁, 男, 博士, 教授, 博士生导师, 主要从事金属有机骨架化合物的合成及性质研究. E-mail:基金资助:
SONG Wei, WANG Liqun, ZENG Shuangli, WANG Li, FAN Yong, XU Jianing*( )
)
Received:2018-03-12
Online:2018-07-10
Published:2018-06-21
Contact:
XU Jianing
E-mail:xujn@mail.jlu.edu.cn
Supported by:摘要:
以镉盐和吡嗪并[2,3-f][1,10]菲啰啉-2,3二羧酸(H2PPDA)配体为主要原料, 在水热条件下合成出2个含镉的配位聚合物. 在反应过程中, H2PPDA配体通过原位反应分解为Dpq配体(Dpq=双-[3,2-d∶2',3'-f]喹喔啉)并与金属中心镉配位. 配位聚合物1和2具有相同的结构式[Cd(Dpq)Cl2], 但呈现出不同的空间结构. X射线单晶衍射分析结果表明它们具有不同的一维链状结构, 并通过配体芳香环间强π-π堆积作用构筑成二维超分子骨架. 此外, 配位聚合物1在室温下展示出良好的固体荧光性质.
中图分类号:
TrendMD:
宋伟, 王力群, 曾双利, 王莉, 范勇, 徐家宁. 镉配位聚合物的原位水热合成、晶体结构及荧光性质. 高等学校化学学报, 2018, 39(7): 1406.
SONG Wei, WANG Liqun, ZENG Shuangli, WANG Li, FAN Yong, XU Jianing. In situ Hydrothermal Synthesis, Crystal Structure and Fluorescence Properties of Two Cadmium Coordination Polymers†. Chem. J. Chinese Universities, 2018, 39(7): 1406.
| Compound | 1 | 2 |
|---|---|---|
| Empirical formula | C14H8Cl2N4Cd | C14H8Cl2N4Cd |
| Formula weight | 415.54 | 415.54 |
| Crystal system | Monoclinic | Orthorhombic |
| Space group | C2/c | Cmcm |
| a/nm | 1.6577(2) | 1.5788(3) |
| b/nm | 1.28344(17) | 1.2109(2) |
| c/nm | 0.71515(9) | 0.69497(14) |
| α/(°) | 90 | 90 |
| β/(°) | 112.901(2) | 90 |
| γ/(°) | 90 | 90 |
| Volume/nm3 | 1.4016(3) | 1.3286(4) |
| Z | 4 | 4 |
| Calculated density(Mg·m-3) | 1.969 | 2.077 |
| Absorption coefficient/mm-1 | 1.935 | 2.041 |
| F(000) | 808 | 808 |
| θ range/(°) | 32.07—28.31 | 3.36—27.43 |
| Goodness-of-fit on F2 | 1.1067 | 1.111 |
| R1,wR2 [I>2σ(I)]* | R1=0.0279, wR2=0.0754 | R1=0.0260, wR2=0.0875 |
| R1,wR2(all data)* | R1=0.0329, wR2=0.0784 | R1=0.0271, wR2=0.0882 |
Table 1 Crystal data and structure refinements for Compounds 1 and 2
| Compound | 1 | 2 |
|---|---|---|
| Empirical formula | C14H8Cl2N4Cd | C14H8Cl2N4Cd |
| Formula weight | 415.54 | 415.54 |
| Crystal system | Monoclinic | Orthorhombic |
| Space group | C2/c | Cmcm |
| a/nm | 1.6577(2) | 1.5788(3) |
| b/nm | 1.28344(17) | 1.2109(2) |
| c/nm | 0.71515(9) | 0.69497(14) |
| α/(°) | 90 | 90 |
| β/(°) | 112.901(2) | 90 |
| γ/(°) | 90 | 90 |
| Volume/nm3 | 1.4016(3) | 1.3286(4) |
| Z | 4 | 4 |
| Calculated density(Mg·m-3) | 1.969 | 2.077 |
| Absorption coefficient/mm-1 | 1.935 | 2.041 |
| F(000) | 808 | 808 |
| θ range/(°) | 32.07—28.31 | 3.36—27.43 |
| Goodness-of-fit on F2 | 1.1067 | 1.111 |
| R1,wR2 [I>2σ(I)]* | R1=0.0279, wR2=0.0754 | R1=0.0260, wR2=0.0875 |
| R1,wR2(all data)* | R1=0.0329, wR2=0.0784 | R1=0.0271, wR2=0.0882 |
| Cd1—N1#1 | 0.23553(2) | Cd1—N1 | 0.23553(2) | Cd1—Cl1#1 | 0.25315(7) |
|---|---|---|---|---|---|
| Cd1—Cl1 | 0.25315(7) | Cd1—Cl1#2 | 0.27349(8) | Cd1—Cl1#3 | 0.27349(8) |
| Cl1—Cd1#3 | 0.27349(8) | ||||
| N1#1—Cd1—Cl1#1 | 93.65(6) | N1—Cd1—Cl1#1 | 160.63(6) | Cl1#1—Cd1—Cl1#3 | 96.40(3) |
| N1#1—Cd1—Cl1 | 160.63(6) | N1—Cd1—Cl1 | 93.65(6) | Cl1#2—Cd1—Cl1#3 | 177.18(3) |
| Cl1#1—Cd1—Cl1 | 103.97(4) | N1#1—Cd1—Cl1#2 | 92.96(6) | Cl1—Cd1—Cl1#2 | 96.40(3) |
| N1—Cd1—Cl1#2 | 84.73(6) | Cl1#1—Cd1—Cl1#2 | 85.35(2) | N1—Cd1—Cl1#3 | 92.96(6) |
| N1#1—Cd1—N1 | 70.33(11) | N1#1—Cd1—Cl1#3 | 84.73(6) | Cl1—Cd1—Cl1#3 | 85.35(2) |
Table 2 Selected bond lengths(nm) and bond angles(°) for compound 1*
| Cd1—N1#1 | 0.23553(2) | Cd1—N1 | 0.23553(2) | Cd1—Cl1#1 | 0.25315(7) |
|---|---|---|---|---|---|
| Cd1—Cl1 | 0.25315(7) | Cd1—Cl1#2 | 0.27349(8) | Cd1—Cl1#3 | 0.27349(8) |
| Cl1—Cd1#3 | 0.27349(8) | ||||
| N1#1—Cd1—Cl1#1 | 93.65(6) | N1—Cd1—Cl1#1 | 160.63(6) | Cl1#1—Cd1—Cl1#3 | 96.40(3) |
| N1#1—Cd1—Cl1 | 160.63(6) | N1—Cd1—Cl1 | 93.65(6) | Cl1#2—Cd1—Cl1#3 | 177.18(3) |
| Cl1#1—Cd1—Cl1 | 103.97(4) | N1#1—Cd1—Cl1#2 | 92.96(6) | Cl1—Cd1—Cl1#2 | 96.40(3) |
| N1—Cd1—Cl1#2 | 84.73(6) | Cl1#1—Cd1—Cl1#2 | 85.35(2) | N1—Cd1—Cl1#3 | 92.96(6) |
| N1#1—Cd1—N1 | 70.33(11) | N1#1—Cd1—Cl1#3 | 84.73(6) | Cl1—Cd1—Cl1#3 | 85.35(2) |
| Cd1—N1#1 | 0.23874(3) | Cd1—N1 | 0.23874(3) | Cd1—Cl1#2 | 0.26266(8) |
|---|---|---|---|---|---|
| Cd1—Cl1#3 | 0.26266(8) | Cd1—Cl1#4 | 0.26266(8) | Cd1—Cl1 | 0.26266(8) |
| Cl1—Cd1#3 | 0.26266(8) | ||||
| N1#1—Cd1—Cl1#2 | 132.38(4) | N1—Cd1—Cl1#2 | 86.67(6) | Cl1#2—Cd1—Cl1 | 82.82(3) |
| N1#1—Cd1—Cl1#3 | 86.67(6) | N1—Cd1—Cl1#3 | 132.38(4) | Cl1#4—Cd1—Cl1 | 136.27(2) |
| Cl1#2—Cd1—Cl1#3 | 136.27(2) | N1#1—Cd1—Cl1#4 | 86.67(6) | N1—Cd1—Cl1#4 | 132.38(4) |
| Cl1#3—Cd1—Cl1 | 81.23(4) | Cl1#2—Cd1—Cl1#4 | 81.23(4) | Cl1#3—Cd1—Cl1#4 | 82.82(3) |
| N1#1—Cd1—N1 | 68.42(16) | N1#1—Cd1—Cl1 | 132.38(4) | N1—Cd1—Cl1 | 86.67(6) |
Table 3 Selected bond lengths(nm) and bond angles(°) for compound 2*
| Cd1—N1#1 | 0.23874(3) | Cd1—N1 | 0.23874(3) | Cd1—Cl1#2 | 0.26266(8) |
|---|---|---|---|---|---|
| Cd1—Cl1#3 | 0.26266(8) | Cd1—Cl1#4 | 0.26266(8) | Cd1—Cl1 | 0.26266(8) |
| Cl1—Cd1#3 | 0.26266(8) | ||||
| N1#1—Cd1—Cl1#2 | 132.38(4) | N1—Cd1—Cl1#2 | 86.67(6) | Cl1#2—Cd1—Cl1 | 82.82(3) |
| N1#1—Cd1—Cl1#3 | 86.67(6) | N1—Cd1—Cl1#3 | 132.38(4) | Cl1#4—Cd1—Cl1 | 136.27(2) |
| Cl1#2—Cd1—Cl1#3 | 136.27(2) | N1#1—Cd1—Cl1#4 | 86.67(6) | N1—Cd1—Cl1#4 | 132.38(4) |
| Cl1#3—Cd1—Cl1 | 81.23(4) | Cl1#2—Cd1—Cl1#4 | 81.23(4) | Cl1#3—Cd1—Cl1#4 | 82.82(3) |
| N1#1—Cd1—N1 | 68.42(16) | N1#1—Cd1—Cl1 | 132.38(4) | N1—Cd1—Cl1 | 86.67(6) |
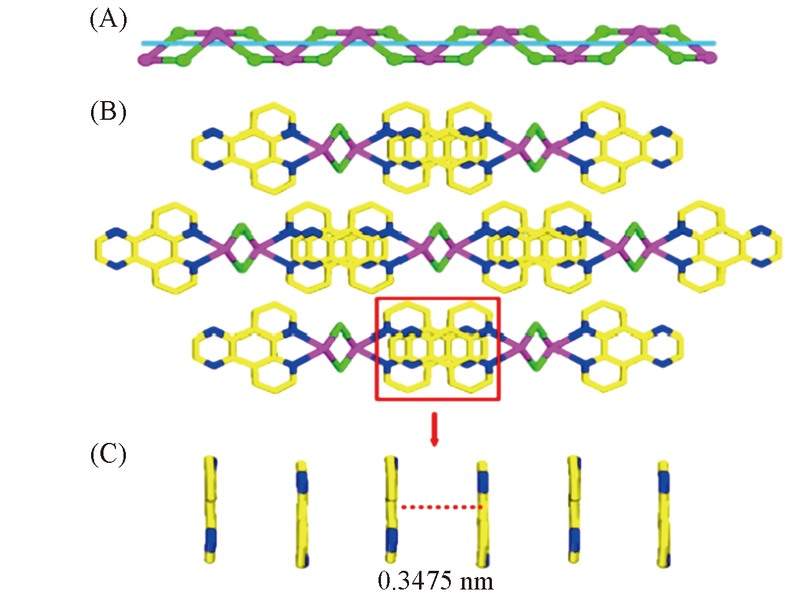
Fig.5 1D chiral chain of compound 2(A), view of framework structure of compound 2 along the z axis and the aromatic stacking effect of 1D chain between adjacent Dpq of compound 2
| [1] | Long J. R., Yaghi O. M., Chem. Soc. Rev., 2009, 38(5), 1213—1214 |
| [2] | Janiak C., Vieth J. K., New J. Chem., 2010, 34(11), 2366—2388 |
| [3] | Allendorf M. D., Bauser C. A., Bhakta R. K., Chem. Soc. Rev., 2009, 38(5), 1330—1352 |
| [4] | Liu B., Zhang R., Pan C. Y., Jiang H. L., Inorg. Chem., 2017, 56(8), 4263—4266 |
| [5] | Bell M., Edwards A. J., Hoskins B. F., Kachab E. H., Robson R., J. Am. Chem. Soc., 1989, 111(10), 3603—3610 |
| [6] | Chen B. L., Eddaoudi M., Hyde S. T., O’Keeffe M., Yaghi O. M., Science, 2001, 291, 1021—1023 |
| [7] | Qi Y. J., Wang Y. H., Hu C. W., Cao M. H., Mao L., Wang E. B., Inorg. Chem., 2003, 42(25), 8519—8523 |
| [8] | Eddaoudi M., Kim J., O’Keeffe M., Yaghi O. M., J. Am. Chem. Soc., 2002, 124(3), 376—377 |
| [9] | Sun J. Y., Weng L. H., Zhou Y. M., Chen J. X., Chen Z. X., Liu Z. C., Zhao D. Y., Angew. Chem. Int. Ed, 2002, 41(23), 4471—4473 |
| [10] | Wang X., Liu G., Zhang J., Chen Y., Lin H., Zheng W., Dalton Trans., 2009, 38(36), 7347—7349 |
| [11] | Wang X., Zheng W., Lin H., Liu G., Chen Y., Fang J., Tetrahedron Lett., 2009, 50(14), 1536—1538 |
| [12] | Wang X. L., Chen Y., Liu G., Lin H., Zhang J., Solid State Sci., 2009, 11(9), 1567—1571 |
| [13] | Wang X. Y., He Y., Zhao L. N., Kong Z. G., Inorg. Chem. Commun., 2011, 14(7), 1186—1189 |
| [14] | Xu C. J., Li B. G., Wan J. T., Bu Z. Y., Spectrochim. Acta A, 2011, 82(1), 159—163 |
| [15] | Wang X. L., Lin H. Y., Liu G. C., Zhao H. Y., Chen B. K., J. Organomet. Chem., 2008, 693(16) , 2767—2774 |
| [16] | Xu Z. L., He Y., Ma S., Wang X. Y., Transition Met. Chem., 2011, 36(6), 585—591 |
| [17] | Yang J., Li G. D., Cao J. J., Yue Q., Li G. H., Chen J. S., Chem. Eur. J., 2007, 13, 3248—3261 |
| [18] | Wei Y., Yu Y., Wu K., Cryst. Growth Des., 2007, 7(11), 2262—2264 |
| [19] | Tao J. Q., Gu Y. L., Zhou X. H., You X. Z., Chin. J. Chem., 2009, 27(7), 1280—1284 |
| [20] | Gaspar A. B., Galet A., Mun M. C., Real J. A., Inorg. Chem., 2006, 45(26), 10431—10433 |
| [21] | Deshpande M. S., Kumbhar A. S., Puranik V. G., Cryst. Growth Des., 2008, 8(6), 1952—1960 |
| [22] | Zapata F., Caballero A., Espinosa A., Tarraga A., Molina P.,Dalton Trans., 2009, (20), 3900—3902 |
| [23] | MacDonnell F. M., Bodige S., Inorg. Chem., 1996, 35(20), 5758—5759 |
| [24] | Campagna S., Serroni S., Bodige S., MacDonnell F. M., Inorg. Chem., 1999, 38(20), 692—701 |
| [25] | Ibrahim K., Mehmet K., Turkish. J. Chem., 2013, 37, 993—1006 |
| [26] | Weng Z. H., Liu D. C., Chen Z. L., Zou H. H., Qin S. N., Liang F. P., Cryst. Growth Des., 2009, 9(9), 4163—4170 |
| [27] | Banisafar A., LaDuca R. L., Inorg. Chim. Acta, 2011, 373, 295—300 |
| [28] | Drozdzewski P., Kubiak M., Polyhedron, 2009, 28(8), 1518—1524 |
| [29] | Hossan A. S. M., Abou-Melha H. M., Refat M. S., Spectrochim. Acta A, 2011, 79(3), 583—593 |
| [30] | Kang Z. X., Fan L. L., Wang S. S., Sun D. F., Xue M., Qiu S. L., Cryst.Eng.Comm., 2017, 19(12), 1601—1606 |
| [31] | Turhan O., Kurtaran R., Namli H., Vib. Spectrosc., 2011, 56(2), 111—115 |
| [32] | Yan L. T., Dai P. C., Wang Y., Gu X., Li L. J., Cao L., Zhao X. B., ACS Appl. Mater. Interfaces, 2017, 9(13), 11642—11650 |
| [33] | Jia J., Xu J. N., Wang S. Y., Wang P. C., Gao L. J., Chai J., Shen L. L., Chen X. B., Fan Y., Wang L., Cryst. Eng. Comm., 2016, 18(37), 7126—7134 |
| [34] | Che C.M., Wan C. W., Lin W. Z., Yu W. Y, Zhou Z. Y., Lai W. Y., Lee S. T.,Chem. Commun., 2001, (8), 721—722 |
| [1] | 王君旸, 刘争, 张茜, 孙春燕, 李红霞. DNA银纳米簇在功能核酸荧光生物传感器中的应用[J]. 高等学校化学学报, 2022, 43(6): 20220010. |
| [2] | 鲁聪, 李振华, 刘金露, 华佳, 李光华, 施展, 冯守华. 一种新的镧系金属有机骨架材料的合成、 结构及荧光检测性质[J]. 高等学校化学学报, 2022, 43(6): 20220037. |
| [3] | 刘晓磊, 陆永强, 游淇, 刘国辉, 姚伟, 胡日茗, 闫纪宪, 崔玉, 杨小凤, 孙国新, 蒋绪川. 基于3-羟基沙利度胺的比率型荧光探针对过氧化氢的检测[J]. 高等学校化学学报, 2022, 43(6): 20220070. |
| [4] | 蒋小康, 周琦, 周恒为. Gd2ZnTiO6∶Dy3+, Eu3+单基质白光荧光粉的制备与发光性能[J]. 高等学校化学学报, 2022, 43(6): 20220029. |
| [5] | 赵永梅, 穆叶舒, 洪琛, 罗稳, 田智勇. 双萘酰亚胺衍生物用于检测水溶液中的苦味酸[J]. 高等学校化学学报, 2022, 43(3): 20210765. |
| [6] | 李巧, 赵洋, 王恩举. 基于芳叉丙二腈的高活性迈克尔系统的吸湿反应及荧光性质[J]. 高等学校化学学报, 2022, 43(3): 20210690. |
| [7] | 田雪琴, 莫争, 丁鑫, 武鹏彦, 王雨, 王健. 方胺功能化荧光金属-有机框架材料的制备及对组氨酸的识别研究[J]. 高等学校化学学报, 2022, 43(2): 20210589. |
| [8] | 唐倩, 但飞君, 郭涛, 兰海闯. 喹啉酮-香豆素类Hg2+比色荧光探针的合成及应用[J]. 高等学校化学学报, 2022, 43(2): 20210660. |
| [9] | 伍泽鑫, 朱渊杰, 王泓中, 王均安, 贺英. 甲基修饰的咔唑/二苯砜基AIE-TADF蓝光材料及其OLED器件[J]. 高等学校化学学报, 2022, 43(11): 20220371. |
| [10] | 王迪, 钟克利, 汤立军, 侯淑华, 吕春欣. 席夫碱共价有机框架的合成及对I ‒ 的识别[J]. 高等学校化学学报, 2022, 43(10): 20220115. |
| [11] | 刘苗, 刘瑞波, 刘巴蒂, 钱鹰. 溶酶体靶向吲哚氟硼二吡咯光敏剂的合成、 双光子荧光成像及光动力治疗[J]. 高等学校化学学报, 2022, 43(10): 20220326. |
| [12] | 李文, 乔珺一, 刘鑫垚, 刘云凌. 含萘基团的锆金属有机骨架材料对水中硝基芳烃爆炸物的荧光检测性能[J]. 高等学校化学学报, 2022, 43(1): 20210654. |
| [13] | 梁宇, 刘欢, 宫丽阁, 王春晓, 王春梅, 于凯, 周百斌. 联咪唑修饰{SiW12O40}杂化物的合成及超级电容性能[J]. 高等学校化学学报, 2022, 43(1): 20210556. |
| [14] | 马鉴新, 刘晓东, 徐娜, 刘国成, 王秀丽. 一种具有发光传感、 安培传感和染料吸附性能的多功能Zn(II)配位聚合物[J]. 高等学校化学学报, 2022, 43(1): 20210585. |
| [15] | 吴季, 张浩, 骆昱晖, 耿吴越, 兰亚乾. 一种具有荧光性质的阳离子Ga⁃MOF用于Fe3+和硝基化合物识别[J]. 高等学校化学学报, 2022, 43(1): 20210617. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||