

高等学校化学学报 ›› 2019, Vol. 40 ›› Issue (10): 2090.doi: 10.7503/cjcu20190199
收稿日期:2019-04-03
出版日期:2019-09-05
发布日期:2019-09-05
通讯作者:
李晓霞
E-mail:ydlixiaoxia@yau.edu.cn
基金资助:
HE Caimei,ZHENG Jingyi,LI Xiaoxia( )
)
Received:2019-04-03
Online:2019-09-05
Published:2019-09-05
Contact:
LI Xiaoxia
E-mail:ydlixiaoxia@yau.edu.cn
Supported by:摘要:
构建了一种新型的基于二硫化钼/纳米金和硫堇/纳米金信号放大的检测17β-雌二醇的电化学适配体传感器. 利用巯基自组装技术将17β-雌二醇的适配体探针DNA固定在二硫化钼/纳米金修饰玻碳电极表面, 与末端带巯基的部分互补DNA链杂交, 将硫堇/纳米金电化学指示剂自组装在杂交后的双链DNA上, 制备了17β-雌二醇电化学适配体传感器. 二硫化钼/纳米金复合材料增加了电极的有效表面积和DNA探针的固定量. 纳米金作为信号物质载体负载硫堇, 实现了电化学指示剂的信号放大. 加入目标物17β-雌二醇后, 目标物与适配体DNA特异性结合, 导致互补DNA链脱落, 双链上结合的硫堇/纳米金电化学指示剂数量减少, 电化学信号降低. 实验结果表明, 在1.0×10 -14~5.0×10 -12 mol/L范围内17β-雌二醇浓度与峰电流的线性关系良好, 检出限为4.2×10 -15 mol/L(S/N=3). 该传感器可望用于其它环境激素类物质的检测.
中图分类号:
TrendMD:
贺彩梅,郑景伊,李晓霞. 基于二硫化钼/纳米金和硫堇/纳米金信号放大的雌二醇电化学适配体传感器. 高等学校化学学报, 2019, 40(10): 2090.
HE Caimei,ZHENG Jingyi,LI Xiaoxia. MoS2-Gold Nanoparticles and Thionine-gold Nanoparticle Based Signal-enhanced Electrochemical Aptasensor for the Detection of 17β-Estradiol †. Chem. J. Chinese Universities, 2019, 40(10): 2090.
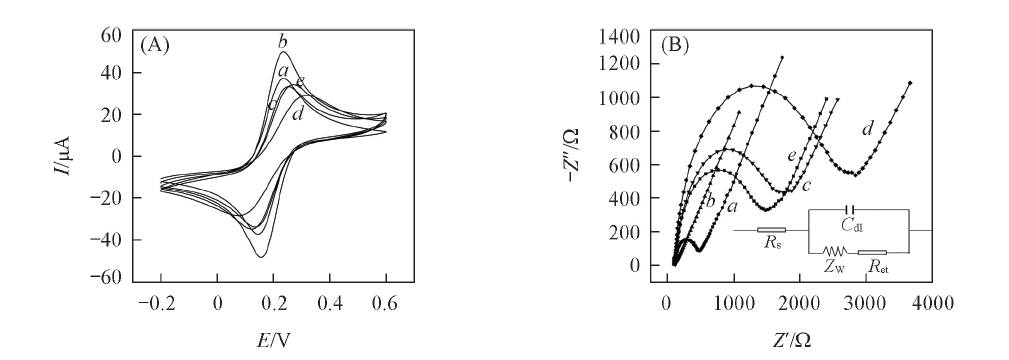
Fig.2 CV(A) and EIS(B) curves of interfaces at different modified electrodes in 5.0 mmol/L [Fe(CN)6]3-/4-/10 mmol/L KCl The scan rate of CV(A) was 50 mV/s, the frequency range of EIS(B) was from 100 kHz to 1.0 Hz and the biased potential was 0.21 V. The inset shows the equivalent circuit diagram applied to fit the impedance spectroscopy. a. GCE; b. GNPs-MoS2/GCE; c. ssDNA/GNPs-MoS2/GCE; d. dsDNA/GNPs-MoS2/GCE; e. GNPs/dsDNA/GNPs-MoS2/GCE.
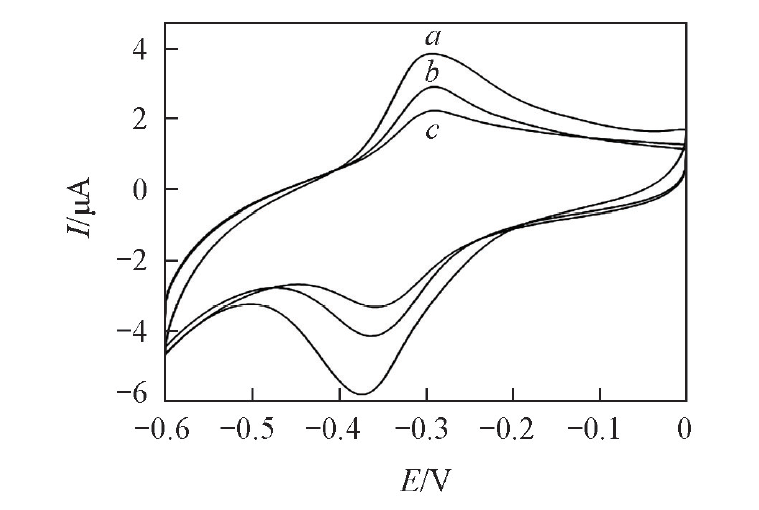
Fig.3 CV response of the electrochemical apta-sensor interacted with different concentrations of E2 in 0.01 mol/L Tris-HCl solution(pH=7.4) cE2/(mol·L-1): a. 0; b. 1.0×10-13; c. 1.0×10-12.
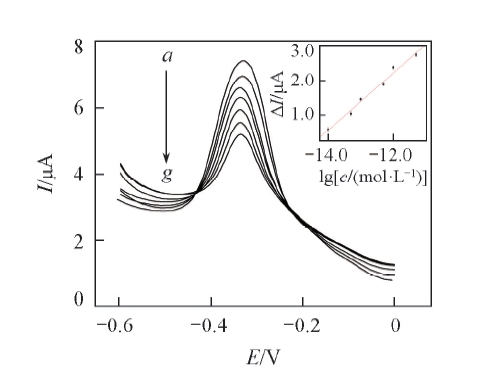
Fig.5 DPV profiles of the aptasensor for the detection different concentrations of E2 and plot of current response vs. E2 concentration(inset) cE2/(mol·L-1): a. 0; b. 1.0×10-14; c. 5.0×10-14; d. 1.0×10-13; e. 5.0×10-13; f. 1.0×10-12 ; g. 5.0×10-12.
| Electrode | Technique | Linear range/ (mol·L-1) | LOD/(mol·L-1) | Sample | Ref. |
|---|---|---|---|---|---|
| Aptamer/poly(Py-co-PAA)/GCE | EIS | 1.0×10-15—1.0×10-6 | 1.0×10-15 | Urine water | [ |
| Aptamer/CuS/GNPs/glucose oxidase/GCE | DPV | 5.0×10-13—5.0×10-9 | 6.0×10-14 | Urine | [ |
| Aptamer /GNPs/WS2/GCE | DPV | 1.0×10-11—1.0×10-8 | 1.0×10-12 | Serum water | [ |
| Aptamer/Au electrode | EIS | 1.0×10-11—1.0×10-8 | 2.0×10-12 | Urine | [ |
| Aptamer /GNPs/CoS/GCE | DPV | 1.0×10-12—1.0×10-9 | 7.0×10-13 | Urine | [ |
| Aptamer/dendritic Au/BDD | EIS | 1.0×10-14 —1.0×10-9 | 5.0×10-15 | Water | [ |
| Aptamer/gold electrode chip | SWV | 1.0×10-11—1.0×10-9 | 1.0×10-13 | [ | |
| Aptamer/CdSe nanoparticles-modified TiO2 nanotube arrays | PEC | 5.0×10-14—1.5×10-11 | 3.3×10-14 | Water | [ |
| Aptamer/ GNPs-MoS2/GCE | DPV | 1.0×10-14—5.0×10-12 | 4.2×10-15 | Water | This work |
Table 1 Comparison of electrochemical aptasensor for the detection of E2*
| Electrode | Technique | Linear range/ (mol·L-1) | LOD/(mol·L-1) | Sample | Ref. |
|---|---|---|---|---|---|
| Aptamer/poly(Py-co-PAA)/GCE | EIS | 1.0×10-15—1.0×10-6 | 1.0×10-15 | Urine water | [ |
| Aptamer/CuS/GNPs/glucose oxidase/GCE | DPV | 5.0×10-13—5.0×10-9 | 6.0×10-14 | Urine | [ |
| Aptamer /GNPs/WS2/GCE | DPV | 1.0×10-11—1.0×10-8 | 1.0×10-12 | Serum water | [ |
| Aptamer/Au electrode | EIS | 1.0×10-11—1.0×10-8 | 2.0×10-12 | Urine | [ |
| Aptamer /GNPs/CoS/GCE | DPV | 1.0×10-12—1.0×10-9 | 7.0×10-13 | Urine | [ |
| Aptamer/dendritic Au/BDD | EIS | 1.0×10-14 —1.0×10-9 | 5.0×10-15 | Water | [ |
| Aptamer/gold electrode chip | SWV | 1.0×10-11—1.0×10-9 | 1.0×10-13 | [ | |
| Aptamer/CdSe nanoparticles-modified TiO2 nanotube arrays | PEC | 5.0×10-14—1.5×10-11 | 3.3×10-14 | Water | [ |
| Aptamer/ GNPs-MoS2/GCE | DPV | 1.0×10-14—5.0×10-12 | 4.2×10-15 | Water | This work |
| Sample | Added/(mol·L-1) | Found/(mol·L-1) | RSD(%) | Recovery(%) |
|---|---|---|---|---|
| 1 | 1.00×10-14 | 1.05×10-14 | 3.7 | 105.0 |
| 2 | 5.00×10-14 | 5.32×10-14 | 4.5 | 106.4 |
| 3 | 1.00×10-13 | 9.89×10-14 | 4.2 | 98.9 |
Table 2 Detection of E2 in tap water samples using the electrochemical aptasensor(n=3)
| Sample | Added/(mol·L-1) | Found/(mol·L-1) | RSD(%) | Recovery(%) |
|---|---|---|---|---|
| 1 | 1.00×10-14 | 1.05×10-14 | 3.7 | 105.0 |
| 2 | 5.00×10-14 | 5.32×10-14 | 4.5 | 106.4 |
| 3 | 1.00×10-13 | 9.89×10-14 | 4.2 | 98.9 |
| [1] | Ying G. G., Kookana R. S., Ru Y. J. , Environ. Int., 2002,28(6), 545— 551 |
| [2] | Ruan A. D., Zong F. J., Zhao Y., Liu C. X., Chen J. , Environ. Toxicol. Chem., 2014,33(4), 768— 775 |
| [3] | Gao R., Hao Y., Zhang L. L., Cui X. H., Liu D., Tang Y. , Anal. Methods, 2014,6(24), 9791— 9799 |
| [4] | Watabe Y., Kubo T., Nishikawa T., Fujita T., Kaya K., Hosoya K. , J. Chromatogr. A, 2006,1120(1/2), 252— 259 |
| [5] | Du L. Y., Ji W., Zhang Y. F., Zhang C.Y. Liu G. F., Wang S. H. , Analyst, 2015,140(6), 2001— 2007 |
| [6] | Moraes F. C., Rossi B., Donatoni M. C., de Oliveira K. T. Pereira E. C. , Anal. Chim. Acta, 2015,881, 37— 43 |
| [7] | Li Y., Xu W. K., Li P., Zhu X. X., Huang Y. F., Zhang J. M. , Chinese J. Anal. Chem., 2018,46(7), 1047— 1054 |
| ( 李颖, 徐文凯, 李苹, 朱小雪, 黄艳凤, 张纪梅 . 分析化学, 2018,46(7), 1047— 1054) | |
| [8] | Li Y. L., Li X. J., Zhang X. Y., Cao J., Zhang J. H., Chen X. Y. , Chinese J. Anal. Chem., 2016,44(10), 1047— 1054 |
| ( 林瑜琳, 李小娟, 张新颖, 曹洁, 张建华, 陈小英 . 分析化学, 2016,44(10), 1547— 1554) | |
| [9] | Özcan A., Topçuoğullari D. , Sens. Actuators B:Chem., 2017,250, 85— 90 |
| [10] | Toh S. Y., Citartan M., Gopinath S. C. B., Tang T. H. , Biosens. Bioelectron., 2015,64, 392— 493 |
| [11] | Jo N., Kim B., Lee S. M., Oh J., Park I. H., Lim K. J., Shin J. S., Yoo K. H. , Biosens. Bioelectron., 2018,102, 164— 170 |
| [12] | Alsager O. A., Kumar S., Zhu B. C., Travas-Sejdic J., McNatty K. P., Hodgkiss J. M. , Anal. Chem., 2015,87(8), 4201— 4209 |
| [13] | Long F., Shi H. C., Wang H. C. , RSC Adv., 2014,4(6), 2935— 2941 |
| [14] | Zhu B. C., Alsager O. A., Kumar S., Hodgkiss J. M., Travas-Sejdic J. , Biosens. Bioelectron., 2015,70, 398— 403 |
| [15] | Huang K. J., Liu Y. J., Zhang J. Z. , Microchim. Acta, 2015,182(1/2), 409— 417 |
| [16] | Huang K. J., Liu Y. J., Zhang J. Z., Liu Y. M. , Anal. Methods, 2014,6(19), 8011— 8017 |
| [17] | Lin Z. Y., Chen L. F., Zhang G. Y., Liu Q. D. Qiu B., Cai Z. C., Chen G. N. , Analyst, 2012,137(4), 819— 822 |
| [18] | Huang K. J., Liu Y. J., Zhang J. Z., Liu Y. M. , Biosens. Bioelectron., 2015,67, 184— 191 |
| [19] | Ke H. Y., Liu M. C., Zhuang L., Li Z. X., Fan L. F., Zhao G. H. , Electrochim. Acta, 2014,137, 146— 153 |
| [20] | Kim Y. S., Jung H. S., Matsuura T., Lee H. Y. , Kawai T., Gua M. B. , Biosens. Bioelectron., 2007,22(11), 2525— 2531 |
| [21] | Fan L. F., Zhao G. H., Shi H. J., Liu M. C. , Wang Y. B., Ke H.Y. , Environ. Sci. Technol., 2014,48(10), 5754— 5761 |
| [22] | Zheng J. Y., Feng R. R., He C. M., Li X. X. , Chem. Res. Chinese Universities, 2018,34(6), 952— 958 |
| [23] | Zhao C. L., Hua M., Zhao X. H., Huang L. L., Feng Y. J., Niu S. P., Fu X. W., Yuan C., Yang Y. H. , Chem. J. Chinese Universities, 2013,34(1), 61— 66 |
| ( 赵春玲, 华梅, 赵晓慧, 黄亮亮, 冯亚娟, 牛司朋, 符雪文, 袁聪, 杨云慧 . 高等学校化学学报, 2013,34(1), 61— 66) | |
| [24] | Li S. Q., Wang X. S., Yang K., Zhao L. , Wu Q. , Huang X. , Huang W. , China Sci. Bull., 2016,61(11), 1222— 1232 |
| ( 李素芹, 王晓珊, 杨凯, 赵丽, 吴琼, 黄晓, 黄维 . 科学通报, 2016,61(11), 1222— 1232) | |
| [25] | Lin X. Y., Ni Y. N., Kokot S. , Sens. Actuators B:Chem., 2016,233, 100— 106 |
| [26] | Su S., Cao W. F., Liu W., Lu Z.W., Zhu D. Chao J., Weng L.X., Wang L.H., Fan C. H., Wang L. H. , Biosens. Bioelectron., 2017,94, 552— 559 |
| [27] | Frens G. , Nature Phys. Sci., 1973,241, 20— 22 |
| [28] | Feng R. R., Hu X. Q., He C. M., Li X. X., Luo X. W., , Anal. Lett., 2017,50(2), 336— 349 |
| [29] | Liu R. Z., Li X. Y. , Chem. J. Chinese Universities, 2017,38(3), 383— 391 |
| ( 刘仁植, 李晓严 . 高等学校化学学报, 2017,38(3), 383— 391) | |
| [30] | Huang K. J., Liu Y. J., Liu Y. M., Wang L. L. , J. Hazardous Mater., 2014,276, 207— 215 |
| [31] | Huang K. J., Liu Y. J., Zhang J. Z., Liu Y. M. , Sens. Actuators B:Chem., 2015,209, 570— 578 |
| [32] | Luo X. W., Du F. J., Wu Y., Gao L. J., Li X. X. , Chinese J. Anal. Chem., 2013,41(11), 1664— 1668 |
| ( 罗贤文, 杜芳静, 吴烨, 高楼军, 李晓霞 . 分析化学, 2013,41(11), 1664— 1668) | |
| [33] | Chen Z. B., Lu M. H. , Sens. Actuators B:Chem., 2018,273, 253— 259 |
| [34] | Gao F., Gao C., He S. Y., Wang Q. X., Wu A. Q., , Biosens. Bioelectron., 2016,81, 15— 22 |
| [35] | Chen X. G., Qian Y., Zhang S. J., Zou X. Y. , Acta Chimica Sinica, 2007,63(4), 337— 343 |
| ( 陈贤光, 钱莹, 张素娟, 邹小勇 . 化学学报, 2007,63(4), 337— 343) | |
| [36] | Wang W., Song L. N., Gao Q., Qi H. L., Zhang C. X. , Electrochem. Commun., 2013,34, 18— 21 |
| [1] | 林高鑫, 王家成. 单原子掺杂二硫化钼析氢催化的进展和展望[J]. 高等学校化学学报, 2022, 43(9): 20220321. |
| [2] | 陈铭苏, 张会茹, 张琪, 刘家琴, 吴玉程. 锂硫电池中钴磷共掺杂MoS2催化性能的第一性原理研究[J]. 高等学校化学学报, 2021, 42(8): 2540. |
| [3] | 张楠, 韩阔, 李悦, 王春茹, 赵凤, 韩冬雪, 牛利. 尖晶石型过渡金属硫化物CuCo2S4与MoS2复合材料的制备及电催化析氢性能[J]. 高等学校化学学报, 2021, 42(4): 1307. |
| [4] | 陈晓煜, 于然波. 纳米二硫化钼的掺杂及催化电解水产氢的研究进展[J]. 高等学校化学学报, 2021, 42(2): 475. |
| [5] | 崔金萍, 陈温贤, 郁非繁, 曹诗雨, 吕维扬, 姚玉元. 碳掺杂六方氮化硼/二硫化钼吸附还原六价铬和助催化降解有机污染物[J]. 高等学校化学学报, 2021, 42(10): 3125. |
| [6] | 王婷婷, 李元, 杨莉莉, 鲍昌昊, 程寒. 碳纤维微电极负载金纳米粒子用于芦荟多糖的在体动态监测[J]. 高等学校化学学报, 2020, 41(1): 87. |
| [7] | 李元, 王婷婷, 李梅, 程寒. 碳纤维微电极表面负载含氧官能团及PDDA-纳米金粒子用于神经递质多巴胺的检测[J]. 高等学校化学学报, 2018, 39(8): 1656. |
| [8] | 代红艳, 杨慧敏, 刘宪, 简选, 郭敏敏, 曹乐乐, 梁镇海. MoS2/石墨烯复合阴极材料的制备及微生物电解池催化产氢性能[J]. 高等学校化学学报, 2018, 39(2): 351. |
| [9] | 冯慧杰, 郑文君. MoS2多级纳米结构的合成及锂离子电池性能[J]. 高等学校化学学报, 2017, 38(7): 1134. |
| [10] | 龚晓庆, 万秀美, 逯丹凤, 高然, 程进, 祁志美. 波长检测型表面等离子体共振传感器对硫堇电聚合成膜的原位分析[J]. 高等学校化学学报, 2017, 38(4): 567. |
| [11] | 刘仁植, 李晓严. MoS2中空纳米球的制备及在超灵敏microRNA电化学生物传感器中的应用[J]. 高等学校化学学报, 2017, 38(3): 383. |
| [12] | 李丹, 吴倩, 刘莉, 孙晓日, 郭蒙, 冯一民. 双子表面活性剂修饰金纳米流体的制备及稳定性[J]. 高等学校化学学报, 2017, 38(10): 1829. |
| [13] | 滕小波, 张春霞, 张颖. 负载金纳米粒子的聚苯乙烯/聚丙烯酸微球的合成及pH响应性能[J]. 高等学校化学学报, 2016, 37(8): 1509. |
| [14] | 赵甜甜, 陈雨晴, 张敏, 王月荣, 章弘扬, 胡坪. 基于纳米金催化的血清尿酸纸芯片的构建及应用[J]. 高等学校化学学报, 2016, 37(5): 829. |
| [15] | 胡杰, 王勇, 倪永年. 基于层状二硫化钼纳米片比色检测亚锡离子[J]. 高等学校化学学报, 2016, 37(3): 448. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||