

高等学校化学学报 ›› 2015, Vol. 36 ›› Issue (5): 821.doi: 10.7503/cjcu20150015
收稿日期:2015-01-07
出版日期:2015-05-10
发布日期:2015-04-20
作者简介:联系人简介: 宋玉民, 女, 教授, 主要从事生物无机化学研究. E-mail: 基金资助:
YANG Meiling1,2, QIN Dongdong1, SONG Yumin1,*( )
)
Received:2015-01-07
Online:2015-05-10
Published:2015-04-20
Contact:
SONG Yumin
E-mail:songym@nwnu.edu.cn
摘要:
用华法林(W)、 阿魏酸(FA)与La, Nd, Ce, Eu的稀土硝酸盐反应合成了4个三元稀土配合物, 并用红外光谱、 热重分析、 元素分析、 X射线粉末衍射和核磁共振波谱等方法对配合物进行了表征, 确定了三元配合物的组成. 在生理条件下测试了该三元配合物的全血凝血时间(CT)、 复钙时间(RT)、 活化部分凝血活酶时间(APTT)、 凝血酶原时间(PT)和生物相容性, 并与稀土华法灵、 稀土阿魏酸二元配合物及配体的抗凝血性质进行了比较. 结果表明, 4个三元稀土配合物均具有比二元配合物和配体更好的抗凝血性质. 生物相容性实验结果表明4个配合物对人肝癌细胞(HepG2)、 人肺癌细胞(A549)和人宫颈癌细胞(HeLa)的活性无明显影响. 通过荧光光谱、 紫外光谱和圆二色谱考察了三元配合物与人血清白蛋白(HSA)之间的相互作用. 结果表明, 配合物可以与HSA相互结合从而增强药物的血溶性, 避免了阿魏酸被氧化而失去原有的药效.
中图分类号:
TrendMD:
杨美玲, 秦冬冬, 宋玉民. 稀土华法林阿魏酸三元配合物的制备及抗凝血作用. 高等学校化学学报, 2015, 36(5): 821.
YANG Meiling, QIN Dongdong, SONG Yumin. Syntheses and Anticoagulant Action of Rare Earth Ternary omplexes with Warfarin and Ferulic Acid†. Chem. J. Chinese Universities, 2015, 36(5): 821.
| Complex | Found(Calcd.)(%) | Λ/(S·cm2·mol-1) | ||
|---|---|---|---|---|
| C | H | RE | ||
| FA-W-La | 49.96(49.66) | 5.30(5.10) | 14.93(14.15) | 29.3 |
| FA-W-Ce | 46.88(46.43) | 5.53(5.02) | 15.68(14.23) | 27.4 |
| FA-W-Nd | 46.01(46.44) | 5.75(5.03) | 16.04(14.58) | 19.6 |
| FA-W-Eu | 49.20(49.43) | 4.11(4.53) | 17.36(15.27) | 18.4 |
Table 1 Elemental analysis and molar conductivity of the complexes
| Complex | Found(Calcd.)(%) | Λ/(S·cm2·mol-1) | ||
|---|---|---|---|---|
| C | H | RE | ||
| FA-W-La | 49.96(49.66) | 5.30(5.10) | 14.93(14.15) | 29.3 |
| FA-W-Ce | 46.88(46.43) | 5.53(5.02) | 15.68(14.23) | 27.4 |
| FA-W-Nd | 46.01(46.44) | 5.75(5.03) | 16.04(14.58) | 19.6 |
| FA-W-Eu | 49.20(49.43) | 4.11(4.53) | 17.36(15.27) | 18.4 |
| Parameter | W-FA-La | W-FA-Nd | W-FA-Ce | W-FA-Eu |
|---|---|---|---|---|
| β | 0.9624 | 0.9790 | 0.9644 | 0.9819 |
| b1/2 | 0.1371 | 0.1025 | 0.1334 | 0.0951 |
| δ | 3.9 | 2.1 | 3.6 | 1.8 |
Table 2 Caculated values of various covalency parameters of the complexes
| Parameter | W-FA-La | W-FA-Nd | W-FA-Ce | W-FA-Eu |
|---|---|---|---|---|
| β | 0.9624 | 0.9790 | 0.9644 | 0.9819 |
| b1/2 | 0.1371 | 0.1025 | 0.1334 | 0.0951 |
| δ | 3.9 | 2.1 | 3.6 | 1.8 |
| Compound | Concentration/(mol·L-1) | CT/min | P |
|---|---|---|---|
| Blank | 0 | 4 | <0.05 |
| FA | 2.0×10-4 | 6 | <0.05 |
| W | 2.0×10-4 | 7 | <0.05 |
| W-Laa | 2.5×10-4 | 11.0 | <0.05 |
| W-Nda | 2.5×10-4 | 13.0 | <0.05 |
| W-Eua | 2.5×10-4 | 9.5 | <0.05 |
| W-Ya | 2.5×10-4 | 8.8 | <0.05 |
| FA-Ndb | 2.5×10-4 | 13.4 | <0.05 |
| FA-Ceb | 2.5×10-4 | 11.3 | <0.05 |
| FA-Eub | 2.5×10-4 | 11.9 | <0.05 |
| W-FA-La | 2.0×10-4 | 25 | <0.05 |
| W-FA-Nd | 2.0×10-4 | 44 | <0.05 |
| W-FA-Ce | 2.0×10-4 | 40 | <0.05 |
| W-FA-Eu | 2.0×10-4 | 42 | <0.05 |
Table 3 Coagulation time of the ligands and complexes
| Compound | Concentration/(mol·L-1) | CT/min | P |
|---|---|---|---|
| Blank | 0 | 4 | <0.05 |
| FA | 2.0×10-4 | 6 | <0.05 |
| W | 2.0×10-4 | 7 | <0.05 |
| W-Laa | 2.5×10-4 | 11.0 | <0.05 |
| W-Nda | 2.5×10-4 | 13.0 | <0.05 |
| W-Eua | 2.5×10-4 | 9.5 | <0.05 |
| W-Ya | 2.5×10-4 | 8.8 | <0.05 |
| FA-Ndb | 2.5×10-4 | 13.4 | <0.05 |
| FA-Ceb | 2.5×10-4 | 11.3 | <0.05 |
| FA-Eub | 2.5×10-4 | 11.9 | <0.05 |
| W-FA-La | 2.0×10-4 | 25 | <0.05 |
| W-FA-Nd | 2.0×10-4 | 44 | <0.05 |
| W-FA-Ce | 2.0×10-4 | 40 | <0.05 |
| W-FA-Eu | 2.0×10-4 | 42 | <0.05 |
| Compound | Concentration/(mol·L-1) | CT/min | P | Compound | Concentration/(mol·L-1) | CT/min | P |
|---|---|---|---|---|---|---|---|
| FA | 2.0×10-5 | 4 | <0.05 | W-FA-Ce | 2.0×10-5 | 31 | <0.05 |
| 2.0×10-4 | 6 | <0.05 | 2.0×10-4 | 40 | <0.05 | ||
| 2.0×10-3 | 7 | <0.05 | 2.0×10-3 | 45 | <0.05 | ||
| W | 2.0×10-5 | 6 | <0.05 | W-FA-Nd | 2.0×10-5 | 42 | <0.05 |
| 2.0×10-4 | 7 | <0.05 | 2.0×10-4 | 44 | <0.05 | ||
| 2.0×10-3 | 10 | <0.05 | 2.0×10-3 | 50 | <0.05 | ||
| W-FA-La | 2.0×10-5 | 20 | <0.05 | W-FA-Eu | 2.0×10-5 | 26 | <0.05 |
| 2.0×10-4 | 25 | <0.05 | 2.0×10-4 | 42 | <0.05 | ||
| 2.0×10-3 | 29 | <0.05 | 2.0×10-3 | 50 | <0.05 |
Table 4 Coagulation time of the ligands and complexes
| Compound | Concentration/(mol·L-1) | CT/min | P | Compound | Concentration/(mol·L-1) | CT/min | P |
|---|---|---|---|---|---|---|---|
| FA | 2.0×10-5 | 4 | <0.05 | W-FA-Ce | 2.0×10-5 | 31 | <0.05 |
| 2.0×10-4 | 6 | <0.05 | 2.0×10-4 | 40 | <0.05 | ||
| 2.0×10-3 | 7 | <0.05 | 2.0×10-3 | 45 | <0.05 | ||
| W | 2.0×10-5 | 6 | <0.05 | W-FA-Nd | 2.0×10-5 | 42 | <0.05 |
| 2.0×10-4 | 7 | <0.05 | 2.0×10-4 | 44 | <0.05 | ||
| 2.0×10-3 | 10 | <0.05 | 2.0×10-3 | 50 | <0.05 | ||
| W-FA-La | 2.0×10-5 | 20 | <0.05 | W-FA-Eu | 2.0×10-5 | 26 | <0.05 |
| 2.0×10-4 | 25 | <0.05 | 2.0×10-4 | 42 | <0.05 | ||
| 2.0×10-3 | 29 | <0.05 | 2.0×10-3 | 50 | <0.05 |
| Compound | RT/min | P | Compound | RT/min | P |
|---|---|---|---|---|---|
| Blank | 2 | <0.05 | FA-Ndb | 11 | <0.05 |
| FA | 4 | <0.05 | FA-Ceb | 10 | <0.05 |
| W | 5 | <0.05 | FA-Eub | 9 | <0.05 |
| W-Laa | 7 | <0.05 | W-FA-La | 10 | <0.05 |
| W-Nda | 10 | <0.05 | W-FA-Nd | 19 | <0.05 |
| W-Eua | 9 | <0.05 | W-FA-Ce | 18 | <0.05 |
| W-Ya | 6 | <0.05 | W-FA-Eu | 15 | <0.05 |
Table 5 Recalcification time of the ligands and complexes
| Compound | RT/min | P | Compound | RT/min | P |
|---|---|---|---|---|---|
| Blank | 2 | <0.05 | FA-Ndb | 11 | <0.05 |
| FA | 4 | <0.05 | FA-Ceb | 10 | <0.05 |
| W | 5 | <0.05 | FA-Eub | 9 | <0.05 |
| W-Laa | 7 | <0.05 | W-FA-La | 10 | <0.05 |
| W-Nda | 10 | <0.05 | W-FA-Nd | 19 | <0.05 |
| W-Eua | 9 | <0.05 | W-FA-Ce | 18 | <0.05 |
| W-Ya | 6 | <0.05 | W-FA-Eu | 15 | <0.05 |
| Compound | c/(mol·L-1) | APTT/s | PT/s | P | Compound | c/(mol·L-1) | APTT/s | PT/s | P |
|---|---|---|---|---|---|---|---|---|---|
| Blank | 0 | 27.50 | 12.40 | <0.05 | W-Eub | 2.0×10-4 | 38.20 | 13.10 | <0.05 |
| FA | 2.0×10-4 | 34.00 | 13.00 | <0.05 | W-Yb | 2.0×10-4 | 37.30 | 13.10 | <0.05 |
| W | 2.0×10-4 | 32.70 | 12.30 | <0.05 | W-FA-La | 2.0×10-4 | 45.50 | 13.60 | <0.05 |
| FA-Nda | 2.0×10-4 | 44.20 | 13.40 | <0.05 | W-FA-Nd | 2.0×10-4 | 48.50 | 14.00 | <0.05 |
| FA-Cea | 2.0×10-4 | 42.20 | 13.10 | <0.05 | W-FA-Ce | 2.0×10-4 | 43.60 | 12.70 | <0.05 |
| FA-Eua | 2.0×10-4 | 43.30 | 13.40 | <0.05 | W-FA-Eu | 2.0×10-4 | 48.20 | 13.90 | <0.05 |
| W-Lab | 2.0×10-4 | 36.70 | 12.50 | <0.05 | Reference | 25—37 | 10—13 | <0.05 | |
| W-Ndb | 2.0×10-4 | 39.50 | 13.30 | <0.05 | valuec |
Table 6 Coagulant activity of the ligands and complexes
| Compound | c/(mol·L-1) | APTT/s | PT/s | P | Compound | c/(mol·L-1) | APTT/s | PT/s | P |
|---|---|---|---|---|---|---|---|---|---|
| Blank | 0 | 27.50 | 12.40 | <0.05 | W-Eub | 2.0×10-4 | 38.20 | 13.10 | <0.05 |
| FA | 2.0×10-4 | 34.00 | 13.00 | <0.05 | W-Yb | 2.0×10-4 | 37.30 | 13.10 | <0.05 |
| W | 2.0×10-4 | 32.70 | 12.30 | <0.05 | W-FA-La | 2.0×10-4 | 45.50 | 13.60 | <0.05 |
| FA-Nda | 2.0×10-4 | 44.20 | 13.40 | <0.05 | W-FA-Nd | 2.0×10-4 | 48.50 | 14.00 | <0.05 |
| FA-Cea | 2.0×10-4 | 42.20 | 13.10 | <0.05 | W-FA-Ce | 2.0×10-4 | 43.60 | 12.70 | <0.05 |
| FA-Eua | 2.0×10-4 | 43.30 | 13.40 | <0.05 | W-FA-Eu | 2.0×10-4 | 48.20 | 13.90 | <0.05 |
| W-Lab | 2.0×10-4 | 36.70 | 12.50 | <0.05 | Reference | 25—37 | 10—13 | <0.05 | |
| W-Ndb | 2.0×10-4 | 39.50 | 13.30 | <0.05 | valuec |
| Compound | c/(mol·L-1) | APTT/s | PT/s | P | Compound | c/(mol·L-1) | APTT/s | PT/s | P |
|---|---|---|---|---|---|---|---|---|---|
| Blank | 0 | 27.50 | 12.40 | <0.05 | W-FA-Nd | 2.0×10-3 | 48.90 | 14.10 | <0.05 |
| FA | 2.0×10-3 | 34.20 | 13.10 | <0.05 | 2.0×10-4 | 48.50 | 14.00 | <0.05 | |
| 2.0×10-4 | 34.00 | 13.00 | <0.05 | 2.0×10-5 | 39.90 | 13.20 | <0.05 | ||
| 2.0×10-5 | 33.60 | 12.70 | <0.05 | W-FA-Ce | 2.0×10-3 | 43.80 | 12.80 | <0.05 | |
| W | 2.0×10-3 | 32.80 | 12.50 | <0.05 | 2.0×10-4 | 43.60 | 12.70 | <0.05 | |
| 2.0×10-4 | 32.70 | 12.30 | <0.05 | 2.0×10-5 | 40.00 | 12.00 | <0.05 | ||
| 2.0×10-5 | 32.10 | 11.90 | <0.05 | W-FA-Eu | 2.0×10-3 | 48.50 | 13.90 | <0.05 | |
| W-FA-La | 2.0×10-3 | 45.80 | 13.70 | <0.05 | 2.0×10-4 | 48.20 | 13.80 | <0.05 | |
| 2.0×10-4 | 45.50 | 13.60 | <0.05 | 2.0×10-5 | 47.80 | 13.10 | <0.05 | ||
| 2.0×10-5 | 0.25 | 45.00 | 13.10 | <0.05 |
Table 7 Coagulant activity of the ligands and complexes with different concentrations
| Compound | c/(mol·L-1) | APTT/s | PT/s | P | Compound | c/(mol·L-1) | APTT/s | PT/s | P |
|---|---|---|---|---|---|---|---|---|---|
| Blank | 0 | 27.50 | 12.40 | <0.05 | W-FA-Nd | 2.0×10-3 | 48.90 | 14.10 | <0.05 |
| FA | 2.0×10-3 | 34.20 | 13.10 | <0.05 | 2.0×10-4 | 48.50 | 14.00 | <0.05 | |
| 2.0×10-4 | 34.00 | 13.00 | <0.05 | 2.0×10-5 | 39.90 | 13.20 | <0.05 | ||
| 2.0×10-5 | 33.60 | 12.70 | <0.05 | W-FA-Ce | 2.0×10-3 | 43.80 | 12.80 | <0.05 | |
| W | 2.0×10-3 | 32.80 | 12.50 | <0.05 | 2.0×10-4 | 43.60 | 12.70 | <0.05 | |
| 2.0×10-4 | 32.70 | 12.30 | <0.05 | 2.0×10-5 | 40.00 | 12.00 | <0.05 | ||
| 2.0×10-5 | 32.10 | 11.90 | <0.05 | W-FA-Eu | 2.0×10-3 | 48.50 | 13.90 | <0.05 | |
| W-FA-La | 2.0×10-3 | 45.80 | 13.70 | <0.05 | 2.0×10-4 | 48.20 | 13.80 | <0.05 | |
| 2.0×10-4 | 45.50 | 13.60 | <0.05 | 2.0×10-5 | 47.80 | 13.10 | <0.05 | ||
| 2.0×10-5 | 0.25 | 45.00 | 13.10 | <0.05 |
| Compound | IC50/(mol·L-1) | Compound | IC50/(mol·L-1) | ||||
|---|---|---|---|---|---|---|---|
| HepG2 | A549 | HeLa | HepG2 | A549 | HeLa | ||
| W | La(NO3)3 | ||||||
| FA | W-FA-La | 10-5 | ≥10-5 | ≥10-5 | |||
| Nd(NO3)3 | 10-3 | Ce(NO3)3 | |||||
| W-FA-Nd | ≥10-4 | 10-4 | ≥10-4 | W-FA-Ce | 10-4 | 10-5 | 10-5 |
| Eu(NO3)3 | cis-PtCl2(NH3)2 | ||||||
| W-FA-Eu | ≥10-4 | ≥10-5 | ≥10-5 | ||||
Table 8 IC50 values of the ligands and complexes on different tumor cells
| Compound | IC50/(mol·L-1) | Compound | IC50/(mol·L-1) | ||||
|---|---|---|---|---|---|---|---|
| HepG2 | A549 | HeLa | HepG2 | A549 | HeLa | ||
| W | La(NO3)3 | ||||||
| FA | W-FA-La | 10-5 | ≥10-5 | ≥10-5 | |||
| Nd(NO3)3 | 10-3 | Ce(NO3)3 | |||||
| W-FA-Nd | ≥10-4 | 10-4 | ≥10-4 | W-FA-Ce | 10-4 | 10-5 | 10-5 |
| Eu(NO3)3 | cis-PtCl2(NH3)2 | ||||||
| W-FA-Eu | ≥10-4 | ≥10-5 | ≥10-5 | ||||
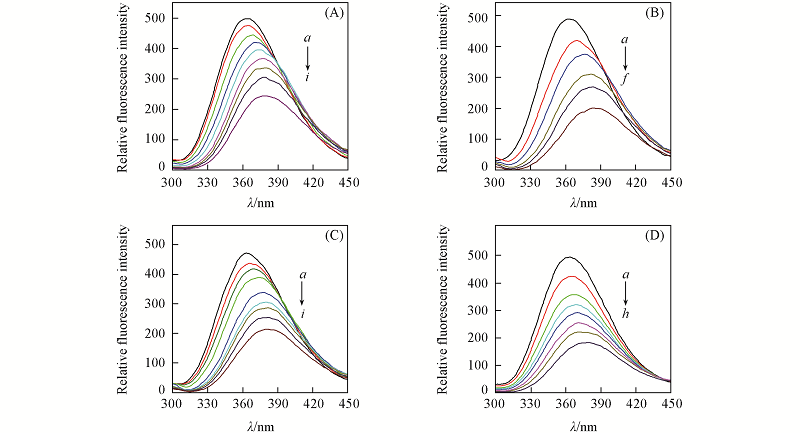
Fig.6 Fluorescence spectra of HSA with W-FA-La(A), W-FA-Ce(B), W-FA-Nd(C) and -FA-Eu(D) cHSA=1.0×10-5 mol/L, ccomplex/(μmol·L-1) from a to i: 0, 20, 40, 60, 80, 100, 120, 140, 160.
| [1] | Guo H. X., Liang C. H., Progress in Biomedical Engineering,2011, 22(3), 44—47 |
| (郭海霞, 梁成浩. 上海生物医学工程, 2011, 22(3), 44—47) | |
| [2] | Xiang Z. B., Huo D. Q., Hou C. J., J. Mol.Diagn. Therapy,2002, 14(4), 25—29 |
| (项昭保, 霍丹群, 侯长军. 现代医学仪器与应用, 2002, 14(4), 25—29) | |
| [3] | Zhu Y. C., Yao K. L., Li Y., Journal of Lanzhou University(Natural Sciences), 2005, 41(6), 61—65 |
| (朱元成, 姚卡玲, 李英. 兰州大学学报(自然科学版), 2005, 41(6), 61—65) | |
| [4] | Song Y. M., Dong Y. L., Fu Y. L., Acta Chim. Sinica,2007, 65(8), 678—682 |
| (宋玉民, 董银龙, 付云龙, 化学学报, 2007, 65(8), 678—682) | |
| [5] | Wang K. J., Luan N. N., SongY. M., Acta Chim. Sinica,2009, 67(10), 1042—1046 |
| (王坤杰, 栾尼娜, 宋玉民. 化学学报, 2009, 67(10), 1042—1046) | |
| [6] | Wang K. J., Song Y. M., Biopolymers,2010, 93(10), 887—892 |
| [7] | Gao Q. K., Wang K. J., Wang C. X., Acta Chim. Sinica,2012, 70(2), 207—211 |
| (高琦宽, 王坤杰, 王喜存. 化学学报, 2012, 70(2), 207—211) | |
| [8] | Eitsuka T., Tatewaki N., Nishida H., Kurata T., Biochem. Bioph. Res. Commun., 2014, 453(3), 606—611 |
| [9] | Woranuch S., Yoksan R., Carbohyd. Poly., 2013, 96(2), 495—502 |
| [10] | Dong Q. R., Bian R. Y., Qu Y., Fang Y. S., J. Tianjin Med., 2011, 39(10), 965—96 |
| (董巧荣, 边如玉, 曲媛, 冯云生. 天津医药, 2011, 39(10), 965—966) | |
| [11] | Wang H. J., Li W. J., Da F. L., Wang J. Y., J. Phys. Chem. B,2008, 112, 2671—2677 |
| [12] | Wang X. D., Jin L. M., Sun Z., Li D. N., Liu T. M., Chem. Res. Chinese Universities,2013, 29(4), 721—723 |
| [13] | Wang P. Y., Bian C. X., Song Y. M., J. Chin. Inorg. Chem., 2012, 28(8), 1609—1616 |
| (王璞玉, 卞常鑫, 宋玉民. 无机化学学报, 2012, 28(8), 1609—1616) | |
| [14] | Sindhu M., Emilia A. T., Food Hydrocolloids,2008, 22, 826—835 |
| [15] | Zhou C. R., An N., Shi X. H., Wang H. F., J. Zhengzhou University,2007, 28(2), 47—48 |
| (周彩荣, 安娜, 石晓华, 王海峰. 郑州大学学报, 2007, 28(2), 47—48) | |
| [16] | Yu X. J., Wu R. H., Song H. Y., Su Q. D., J. Analy. Sci., 2003, 19(2), 101—104 |
| (于锡娟, 伍荣护, 宋慧宇, 苏庆德. 分析科学学报, 2003, 19(2), 101—104) | |
| [17] | Mogren M., Al-Farhan K., Hasanein A. A., J. Saudi.Chem. Soc., 2013, 17(1), 87—95 |
| [18] | Song Y. M., Bian C. X., Wang P. Y., Chem. & Bioeng., 2011, 28(12), 32—34 |
| (宋玉民, 卞常鑫, 王璞玉. 化学与生物工程, 2011, 28(12), 32—34) | |
| [19] | Fan X.L., Physiology, People’s Medical Publishing House, Beijing, 2002, 54—60 |
| (樊小力. 生理学, 北京:人民卫生出版社, 2002, 54—60) | |
| [20] | Zhou H.H., Pharmacology, Science Press, Beijing, 2007, 37, 318—320 |
| (周宏灏. 药理学, 北京:科学出版社, 2007, 37, 318—320) | |
| [21] | Inorganic Chemisty Teaching Group of Beijing Normal University, Huazhong Normal University and Nanjing Normal University, Inorganic Chemistry, Higher Education Press, Beijing, 2003, 648, 816 |
| (北京师范大学、 华中师范大学、 南京师范大学无机化学教研室. 无机化学, 北京: 高等教育出版社, 2003, 648; 816) | |
| [22] | Chen Y., Xu C., Su J. C., J. Chin. Inorg. Chem., 2011, 27(4), 625—630 |
| (陈于, 徐灿, 苏佳灿. 无机化学学报, 2011, 27(4), 625—630) | |
| [23] | Song Y. M., Liu Z., Wang K. J., Acta Chim. Sinica,2010, 68(21), 2191—2198 |
| (宋玉民, 刘哲, 王坤杰. 化学学报, 2010, 68(21), 2191—2198) | |
| [24] | Zhao F., Huang C. F., Liang H., J.Chin. Anal. Chem., 2006, 39(3), 401—404 |
| (赵芳, 黄超峰, 梁慧. 分析化学, 2006, 39(3), 401—404) | |
| [25] | Kong D. L., Wei B., Zhou S. Y., Yang H. S., Jiang Y., Chem. Res. Chinese Universities,2013, 29(6), 1055—1058 |
| [26] | Yang S. P., Han L. J., Pang Y., Wang D. Q., Wang N. N., Wang T., Chem. J. Chinese Universities,2013, 34(2), 364—374 |
| (杨树平, 韩立军, 潘燕, 王大奇, 王南南, 王婷. 高等学校化学学报, 2013, 34(2), 364—374) | |
| [27] | Huang Y., Wang J., Guo G. Y., Tao Z., Xue S. F., Zhu Q. J., Zhou Q. D., Chem. J. Chinese Universities,2013, 34(2), 375—380 |
| (黄英, 王娟, 郭改英, 陶朱, 薛赛凤, 祝黔江, 周清娣. 高等学校化学学报, 2013, 34(2), 375—380) | |
| [28] | Zhang G. W., Wang L., Pan J. H., J.Agri.Food Chem., 2012, 60, 2721—2729 |
| [1] | 鲁聪, 李振华, 刘金露, 华佳, 李光华, 施展, 冯守华. 一种新的镧系金属有机骨架材料的合成、 结构及荧光检测性质[J]. 高等学校化学学报, 2022, 43(6): 20220037. |
| [2] | 周永辉, 李尧, 吴雨轩, 田晶, 徐龙权, 费旭. 一种新型光致发光自愈合水凝胶的合成[J]. 高等学校化学学报, 2022, 43(2): 20210606. |
| [3] | 魏闯宇, 陈艳丽, 姜建壮. 基于乙硫基取代的三层酞菁铕二聚体修饰ITO电极构筑电化学多巴胺和尿酸传感器[J]. 高等学校化学学报, 2022, 43(1): 20210582. |
| [4] | 韩宗甦, 于晓泳, 闵辉, 师唯, 程鹏. 一个基于偶氮六酸的稀土金属-有机框架[J]. 高等学校化学学报, 2022, 43(1): 20210342. |
| [5] | 李梦硕, 张静, 刘丹, 朱亚先, 张勇. 芘与人血清白蛋白和牛血清白蛋白结合位点微环境极性的差异[J]. 高等学校化学学报, 2021, 42(3): 731. |
| [6] | 张爱芹, 王嫚, 申刚义, 金军. 多溴联苯醚与人血清白蛋白相互作用的表面等离子体共振及分子对接[J]. 高等学校化学学报, 2020, 41(9): 2054. |
| [7] | 梁龙琪, 陈彩玲, 于影, 李雨昕, 李春光, 施展. 氨基酸包覆的YVO4∶Eu纳米粒子的合成、 发光及细胞成像性能[J]. 高等学校化学学报, 2020, 41(3): 425. |
| [8] | 李观俊, 龙腊生, 孔祥建, 郑兰荪. 稀土-钛氧簇合物的研究进展[J]. 高等学校化学学报, 2020, 41(12): 2577. |
| [9] | 冉诗雅, 沈海峰, 李晓楠, 王子路, 郭正虹, 方征平. 三氟甲烷磺酸稀土盐对聚丙烯热稳定性的影响及机理[J]. 高等学校化学学报, 2019, 40(6): 1333. |
| [10] | 李冰, 王学敏, 白凤英, 刘淑清. 稀土氮杂环配合物的合成、 结构及抑菌活性[J]. 高等学校化学学报, 2019, 40(4): 632. |
| [11] | 梁东磊, 宋秋生, 姚玉田, 刘贲. 上转换荧光响应性复合纳米凝胶的制备及荧光能量传递行为[J]. 高等学校化学学报, 2019, 40(3): 583. |
| [12] | 崔胜峰, 万敬伟, 周成合. 地西泮与乙醇协同作用机制的荧光光谱分析[J]. 高等学校化学学报, 2018, 39(6): 1178. |
| [13] | 张岩, 张盛明, 方桂珍. Ce掺杂固体酸活化的碱木质素的抗氧化性能[J]. 高等学校化学学报, 2018, 39(6): 1255. |
| [14] | 张德春, 许奇炜, 李夏. 由2,2'-联苯醚二甲酸和1H-咪唑并[4,5-f][1,10]-邻菲罗啉构筑的稀土配合物的荧光光谱及对氨的荧光传感[J]. 高等学校化学学报, 2018, 39(12): 2611. |
| [15] | 唐可云, 李萝园, 付立民, 艾希成, 张建平. 晶体基质对稀土上转换纳米材料中能量转换机理的影响[J]. 高等学校化学学报, 2018, 39(10): 2136. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||