

高等学校化学学报 ›› 2023, Vol. 44 ›› Issue (12): 20230372.doi: 10.7503/cjcu20230372
收稿日期:2023-08-17
出版日期:2023-12-10
发布日期:2023-10-08
通讯作者:
郭景富
E-mail:guojf217@nenu.edu.cn
作者简介:第一联系人:共同第一作者.
基金资助:
PAN Jiazheng1, SUN Xiaoqi1, REN Aimin2, GUO Jingfu1( )
)
Received:2023-08-17
Online:2023-12-10
Published:2023-10-08
Contact:
GUO Jingfu
E-mail:guojf217@nenu.edu.cn
Supported by:摘要:
n型半导体材料在逻辑互补电路中必不可少, 但由于多数n型有机半导体材料空气稳定性差、 迁移率较低, 其发展相对滞后. 本文基于几种典型的不同π核扩展的萘四甲酰基二酰亚胺(NDI)有机半导体材料, 利用第一性原理计算分析了其电荷传输性质, 分别从单分子结构特征、 分子间堆积方式以及分子间相互作用等方面阐明不同核心结构对载流子传输性质的影响. 结果表明, 所研究分子均具有良好的空气稳定性, 并表现为电子传输性. 其中, 长轴π扩展的分子A2具有较高的电子亲和势, 其空气稳定性最好. 其次, 沿长轴/短轴π扩展的NDI有机半导体的重组能均降低, 但二者重组能降低的起因明显不同: 相比于A1分子, 沿短轴π扩展的A2分子在高频区的振动受到有效的抑制, 从而重组能大幅下降; 而沿长轴π扩展的A3与A4分子则在高低频区的振动均受到抑制, 使重组能降低. 另外, 不同的分子堆积对传输影响较大, 发现沿长轴π扩展的A3和A4具有较小的短轴滑移, 表现为二维传输材料, 二维平均电子迁移率分别约为0.06与0.15 cm2·V‒1·s‒1; 沿短轴π扩展的A2分子具有较大的短轴滑移, 因此表现为一维传输材料, 其一维电子迁移率高达0.96 cm2·V‒1·s‒1.
中图分类号:
TrendMD:
潘佳峥, 孙晓琦, 任爱民, 郭景富. 基于不同π核扩展方式萘四甲酰基二酰亚胺有机半导体电荷传输性质的理论研究. 高等学校化学学报, 2023, 44(12): 20230372.
PAN Jiazheng, SUN Xiaoqi, REN Aimin, GUO Jingfu. Theoretical Study of the Charge Transport Properties of Naphthalene Tetracarboxylic Diimide Organic Semiconductors Based on Different π-Core Extensions. Chem. J. Chinese Universities, 2023, 44(12): 20230372.
| Molecule | Gas(QM⁃Model) | Solid(QM/MM⁃Model) | X⁃ray | |||
|---|---|---|---|---|---|---|
| α1/(°) | α2/(°) | α1/(°) | α2/(°) | α1/(°) | α2/(°) | |
| A1 | -0.79 | 0.92 | 2.14 | 2.31 | 2.14 | 2.32 |
| A2 | 13.52 | 16.62 | 14.70 | 17.25 | 13.58 | 19.29 |
| A3 | 0.79 | -0.82 | 2.44 | 2.89 | 2.44 | 2.90 |
| A3** | 0.77 | -0.83 | 0.14 | 0.21 | 0.13 | 0.21 |
| A4 | 0.82 | -0.82 | 1.62 | -1.80 | 1.63 | -1.81 |
Table 1 Dihedral angles( α ) between the acyl group and the central benzene ring of the series of molecules*
| Molecule | Gas(QM⁃Model) | Solid(QM/MM⁃Model) | X⁃ray | |||
|---|---|---|---|---|---|---|
| α1/(°) | α2/(°) | α1/(°) | α2/(°) | α1/(°) | α2/(°) | |
| A1 | -0.79 | 0.92 | 2.14 | 2.31 | 2.14 | 2.32 |
| A2 | 13.52 | 16.62 | 14.70 | 17.25 | 13.58 | 19.29 |
| A3 | 0.79 | -0.82 | 2.44 | 2.89 | 2.44 | 2.90 |
| A3** | 0.77 | -0.83 | 0.14 | 0.21 | 0.13 | 0.21 |
| A4 | 0.82 | -0.82 | 1.62 | -1.80 | 1.63 | -1.81 |
| Molecule | EHOMO/eV | ELUMO/eV | Eg/eV | EHOMO(exp)/eV | ELUMO(exp)/eV | EA(a)/eV |
|---|---|---|---|---|---|---|
| A1 | -7.31 | -3.71 | 3.60 | — | -3.89 | 2.22 |
| A2 | -6.13 | -4.04 | 2.09 | — | -4.13 | 2.54 |
| A3 | -6.69 | -3.65 | 3.04 | -6.43 | -3.69 | 2.11 |
| A3** | -6.34 | -3.27 | 3.07 | — | — | 1.77 |
| A4 | -6.30 | -3.81 | 2.49 | — | — | 2.33 |
| Naphthalene | — | -1.34 | — | — | — | — |
| Tetracene | — | -2.40 | — | — | — | — |
| Pyrene | — | -1.76 | — | — | — | — |
| Perylene | — | -2.19 | — | — | — | — |
Table 2 Calculated electronic structures for the NDI derivatives and reference molecule at the level of B3LYP/6-311++G(d,p)//B3LYP/6-31G(d,p)
| Molecule | EHOMO/eV | ELUMO/eV | Eg/eV | EHOMO(exp)/eV | ELUMO(exp)/eV | EA(a)/eV |
|---|---|---|---|---|---|---|
| A1 | -7.31 | -3.71 | 3.60 | — | -3.89 | 2.22 |
| A2 | -6.13 | -4.04 | 2.09 | — | -4.13 | 2.54 |
| A3 | -6.69 | -3.65 | 3.04 | -6.43 | -3.69 | 2.11 |
| A3** | -6.34 | -3.27 | 3.07 | — | — | 1.77 |
| A4 | -6.30 | -3.81 | 2.49 | — | — | 2.33 |
| Naphthalene | — | -1.34 | — | — | — | — |
| Tetracene | — | -2.40 | — | — | — | — |
| Pyrene | — | -1.76 | — | — | — | — |
| Perylene | — | -2.19 | — | — | — | — |
| Molecule | λAP/eV | λNM/eV | λlow/eV | λhigh/eV |
|---|---|---|---|---|
| A1 | 346.4 | 353.5 | 78.5 | 267.9 |
| A2 | 274.6 | 274.8 | 90.8 | 183.8 |
| A3 | 289.2 | 289.9 | 61.6 | 227.6 |
| A3** | 248.2 | 248.6 | 66.1 | 182.1 |
| A4 | 268.9 | 269.1 | 50.6 | 218.3 |
Table 3 Calculated total intramolecular electronic reorganization energies( λAP/ λNM), and distribution in the high and low frequency regions( λlow/ λhigh) with QM/MM model for studied NDI derivatives
| Molecule | λAP/eV | λNM/eV | λlow/eV | λhigh/eV |
|---|---|---|---|---|
| A1 | 346.4 | 353.5 | 78.5 | 267.9 |
| A2 | 274.6 | 274.8 | 90.8 | 183.8 |
| A3 | 289.2 | 289.9 | 61.6 | 227.6 |
| A3** | 248.2 | 248.6 | 66.1 | 182.1 |
| A4 | 268.9 | 269.1 | 50.6 | 218.3 |
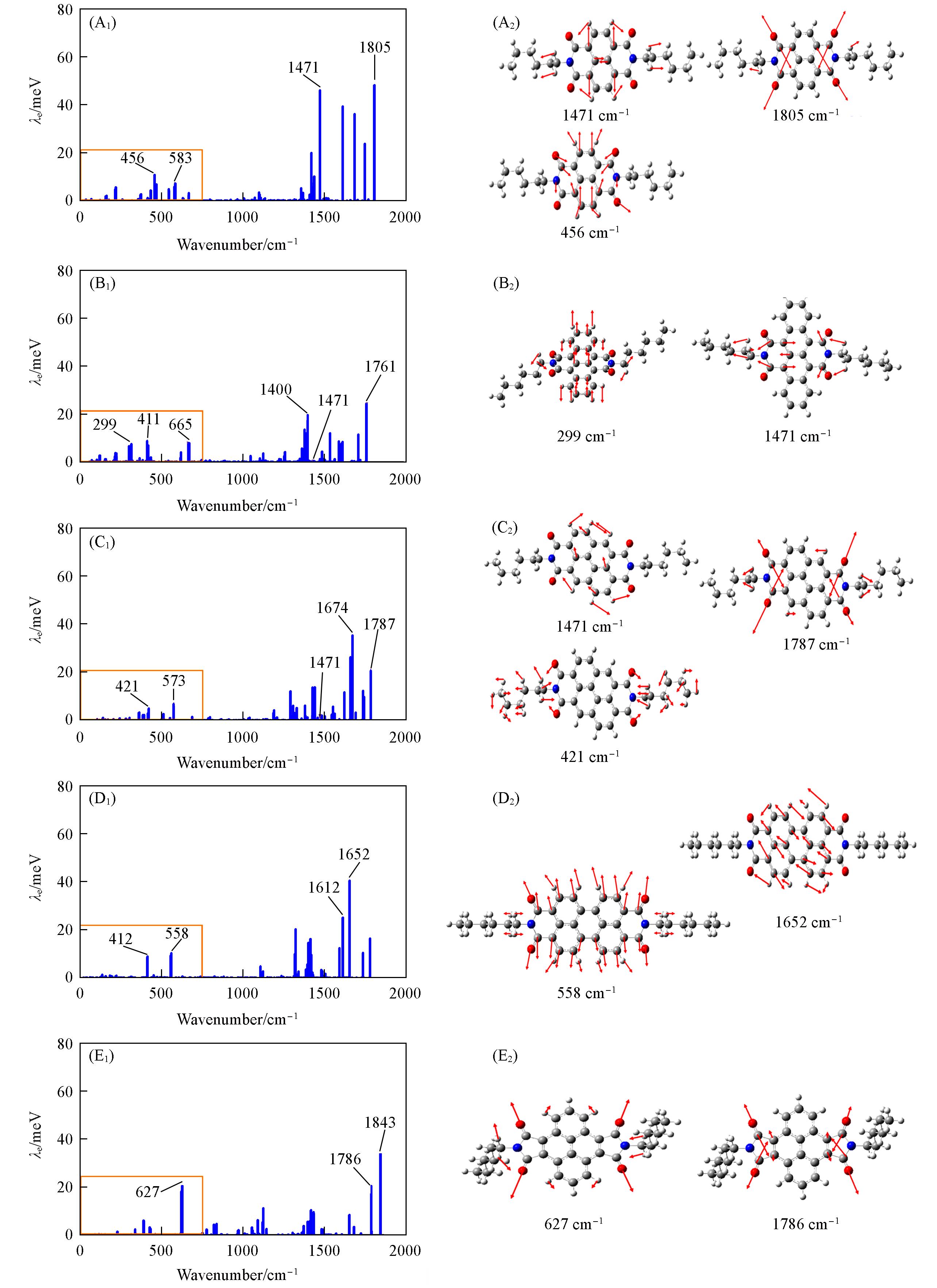
Fig.4 Contribution of each vibration mode to the electronic reorganization energy(A1—E1) and the specific vibrational modes of the molecules corresponding to the vibrational frequencies(A2—E2) of A1(A), A2(B), A3(C), A4(D) and A3**(E)
| Path | A1 | A2 | A3 | A3** | A4 | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| d/nm | Ve/meV | Vh/meV | d/nm | Ve/meV | Vh/meV | d/nm | Ve/meV | Vh/meV | d/nm | Ve/meV | Vh/meV | d/nm | Ve/meV | Vh/meV | |
| 1 | 4.823 | 65.6 | 30.7 | 5.037 | 91.8 | 58.7 | 4.792 | 65.1 | 63.0 | 4.795 | 26.2 | 7.3 | 4.730 | 33.0 | 113.2 |
| 2 | 8.304 | 28.4 | 8.3 | 10.034 | 5.3 | 4.2 | 9.034 | 10.3 | 36.8 | 8.164 | 8.7 | 36.1 | 9.272 | 41.3 | 2.8 |
| 3 | 9.383 | 24.3 | 1.1 | 11.314 | 4.6 | 6.3 | 9.710 | 6.5 | 5.8 | 10.458 | 10.9 | 1.9 | 11.997 | 10.5 | 0.3 |
Table 4 Electron/hole transfer integrals(Ve /Vh) for the studied molecules, and the centre-of-mass distances(d) between neighbouring dimers
| Path | A1 | A2 | A3 | A3** | A4 | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| d/nm | Ve/meV | Vh/meV | d/nm | Ve/meV | Vh/meV | d/nm | Ve/meV | Vh/meV | d/nm | Ve/meV | Vh/meV | d/nm | Ve/meV | Vh/meV | |
| 1 | 4.823 | 65.6 | 30.7 | 5.037 | 91.8 | 58.7 | 4.792 | 65.1 | 63.0 | 4.795 | 26.2 | 7.3 | 4.730 | 33.0 | 113.2 |
| 2 | 8.304 | 28.4 | 8.3 | 10.034 | 5.3 | 4.2 | 9.034 | 10.3 | 36.8 | 8.164 | 8.7 | 36.1 | 9.272 | 41.3 | 2.8 |
| 3 | 9.383 | 24.3 | 1.1 | 11.314 | 4.6 | 6.3 | 9.710 | 6.5 | 5.8 | 10.458 | 10.9 | 1.9 | 11.997 | 10.5 | 0.3 |
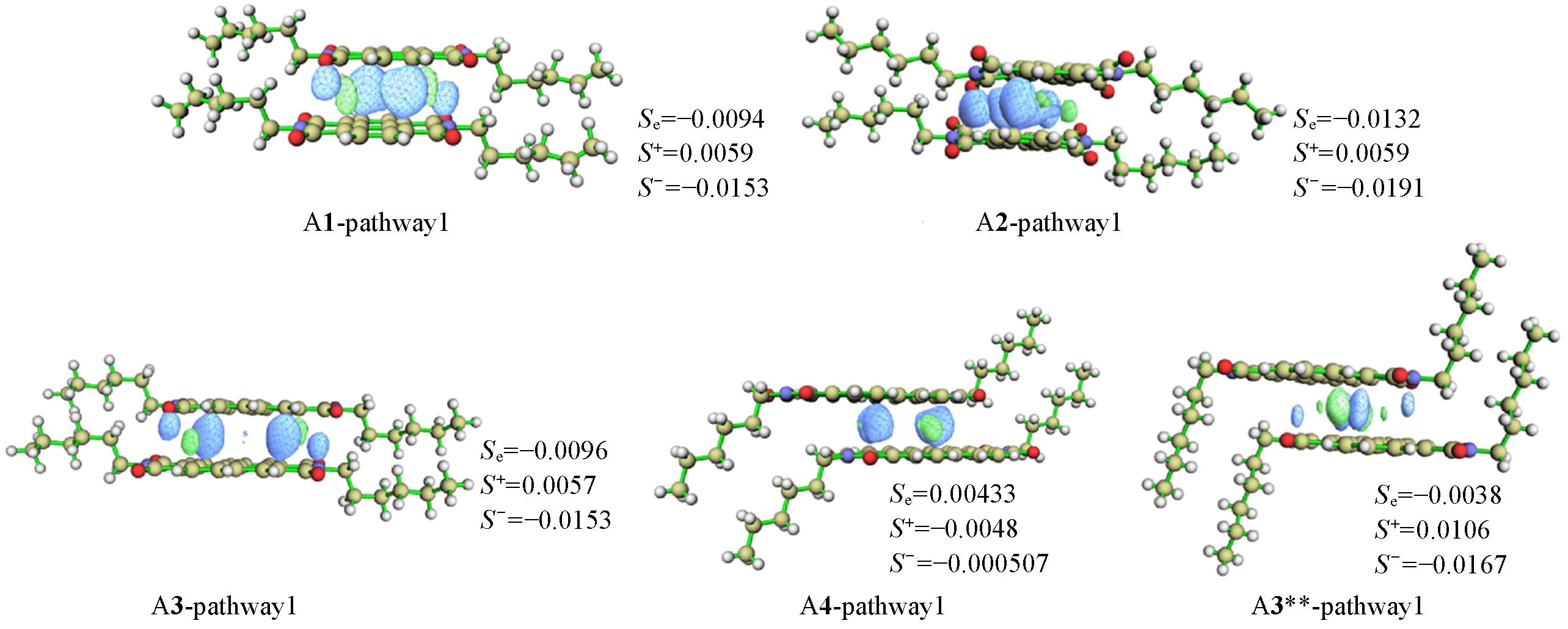
Fig.7 Orbital overlap integral for moleculesGreen represents in-phase positive overlap(S+) and orange represents in reverse phase overlap(S-); Se is electron overlap integral values.
| Molecule | Eelec/(kJ·mol-1) | Eind/(kJ·mol-1) | Edisp/(kJ·mol-1) | Eexch/(kJ·mol-1) | Eattraction/Erepulsion | ESCS-SAPT0/(kJ·mol-1) |
|---|---|---|---|---|---|---|
| A1 | -46.94(16.55%) | -13.35(4.70%) | -132.22(46.60%) | 91.17(32.15%) | 2.11 | -101.30 |
| A2 | -81.13(16.63%) | -20.21(4.15%) | -224.56(46.04%) | 161.80(33.18%) | 2.01 | -164.10 |
| A3 | -59.29(15.34%) | -15.94(4.12%) | -184.68(47.80%) | 126.40(32.71%) | 2.05 | -133.51 |
| A3** | -45.48(12.51%) | -12.68(3.48%) | -193.93(53.29%) | 111.76(30.71%) | 2.26 | -140.33 |
| A4 | -60.38(12.32%) | -16.74(3.42%) | -251.84(51.40%) | 161.04(32.86%) | 2.04 | -167.91 |
Table 5 Calculated intermolecular interaction energy of the nearest dimer for molecules A1—A4 and its corresponding energy decompositions by SAPT0
| Molecule | Eelec/(kJ·mol-1) | Eind/(kJ·mol-1) | Edisp/(kJ·mol-1) | Eexch/(kJ·mol-1) | Eattraction/Erepulsion | ESCS-SAPT0/(kJ·mol-1) |
|---|---|---|---|---|---|---|
| A1 | -46.94(16.55%) | -13.35(4.70%) | -132.22(46.60%) | 91.17(32.15%) | 2.11 | -101.30 |
| A2 | -81.13(16.63%) | -20.21(4.15%) | -224.56(46.04%) | 161.80(33.18%) | 2.01 | -164.10 |
| A3 | -59.29(15.34%) | -15.94(4.12%) | -184.68(47.80%) | 126.40(32.71%) | 2.05 | -133.51 |
| A3** | -45.48(12.51%) | -12.68(3.48%) | -193.93(53.29%) | 111.76(30.71%) | 2.26 | -140.33 |
| A4 | -60.38(12.32%) | -16.74(3.42%) | -251.84(51.40%) | 161.04(32.86%) | 2.04 | -167.91 |
| Molecule | μ1Dmax/(cm2·V‒1·s‒1) | μ2D/(cm2·V‒1·s‒1) | μexp/(cm2·V‒1·s‒1) |
|---|---|---|---|
| A1 | 0.19 | 0.07 | 0.70[ |
| A2 | 0.96 | 0.02 | 0.03[ |
| A3 | 0.32 | 0.06 | — |
| A3** | 0.10 | 0.03 | 0.51[ |
| A4 | 0.71 | 0.15 | — |
Table 6 Simulated electron mobilities of all compounds investigated and available experimental values*
| Molecule | μ1Dmax/(cm2·V‒1·s‒1) | μ2D/(cm2·V‒1·s‒1) | μexp/(cm2·V‒1·s‒1) |
|---|---|---|---|
| A1 | 0.19 | 0.07 | 0.70[ |
| A2 | 0.96 | 0.02 | 0.03[ |
| A3 | 0.32 | 0.06 | — |
| A3** | 0.10 | 0.03 | 0.51[ |
| A4 | 0.71 | 0.15 | — |
| 1 | Yun H. J., Lee G. B., Chung D. S., Kim Y. H., Kwon S. K., Adv. Mater., 2014, 26(38), 6612—6616 |
| 2 | Dou L., Liu Y., Hong Z., Li G., Yang Y., Chem. Rev., 2015, 115(23), 12633—12665 |
| 3 | Panigrahi D., Hayakawa R., Wakayama Y., Adv. Funct. Mater., 2023, 33(20), 2213899 |
| 4 | Liu X., Anderson C. L., Liu Y., Acc. Chem. Res., 2023, 56(12), 1669—1682 |
| 5 | Zhang T., Xiao Y., Wang H., Kong S., Huang R., Au V. K. M., Yu T., Huang W., Angew. Chem. Int. Ed., 2023, e202301896 |
| 6 | Prache O., Displays., 2001, 22(2), 49—56 |
| 7 | Lee S. Y., Yasuda T., Yang Y. S., Zhang Q. S., Adachi C., Angew. Chem. Int. Ed., 2014, 53(25), 6402—6406 |
| 8 | Zhang H., Wang C., Li X., Jing J., Sun Y., Liu Y., Sol. Energy, 2017, 157(15), 71—80 |
| 9 | Anthopoulos T. D., Setayesh S., Smits E., Clle M., Leeuw D. M. D., Adv. Mater., 2010, 18(14), 1900—1904 |
| 10 | Jedaa A., Burkhardt M., Zschieschang U., Klauk H., Habich D., Schmid G., Halik M., Org. Electronics, 2009, 10(8), 1442—1447 |
| 11 | Tang M. L., Reichardt A. D., Wei P., Bao Z., J. Am. Chem. Soc., 2009, 131(14), 5264—5273 |
| 12 | Haddon R. C., Chi X., Itkis M. E., Anthony J. E., Eaton D. L., Siegrist T., Mattheus C. C., Palstra T. T. M., J. Phys. Chem. B, 2002, 106(33), 8288—8292 |
| 13 | Jones B. A., Facchetti A., Wasielewski M. R., Marks T. J., J. Am. Chem. Soc., 2007, 129(49), 15259—15278 |
| 14 | Dou J. H., Zheng Y. Q., Yao Z. F., Yu Z. A., Lei T., Shen X., Luo X. Y., Sun J., Zhang S. D., Ding Y. F., Han G., Yi Y., Wang J. Y., Pei J., J. Am. Chem. Soc., 2015, 137(50), 15947—15956 |
| 15 | Bhosale S. V., Jani C. H., Langford S. J., Chem. Soc. Rev., 2008, 37(2), 331—342 |
| 16 | Sakai N., Mareda J., Vauthey E., Matile S., Chem. Commun., 2010, 46(24), 4225—4237 |
| 17 | Jia T., Li Z., Ying L., Jia J., Fan B., Zhong W., Pan F., He P., Chen J., Huang F., Cao Y., Macromol. Rapid. Comm., 2018, 39(14), 1700765 |
| 18 | Singh T. B., Erten S., Günes S., Zafer C., Turkmen G., Kuban B., Teoman Y., Sariciftci N. S., Icli S., Org. Electron., 2006, 7(6), 480—489 |
| 19 | Shukla D., Nelson S. F., Freeman D. C., Rajeswaran M., Ahearn W. G., Meyer D. M., Carey J. T., Chem. Mater., 2008, 20(24), 7486—7491 |
| 20 | Katsuta S., Tanaka K., Maruya Y., Mori S., Masuo S., Okujima T., Uno H., Nakayama K. I., Yamada H., Chem. Mater., 2011, 47(36), 10112—10114 |
| 21 | Wu Z. H., Huang Z. T., Guo R. X., Sun C. L., Chen L. C., Sun B., Shi Z. F., Shao X., Li H., Zhang H. L., Angew. Chem. Int. Ed., 2017, 56(42), 13031—13035 |
| 22 | Li Y., Yao Z., Xie J., Han H., Yang G., Bai X., Pei J., Zhao D., J. Mater. Chem. C, 2021, 9(24), 7599—7606 |
| 23 | Pitchaimani J., Kundu A., Anthony S. P., Moon D., Madhu V., Chem. Select., 2020, 5(6), 2070—2074 |
| 24 | Cheng Y. C., Silbey R. J., da Silva Filho D. A., Calbert J. P., Cornil J., Brédas J. L., J. Mater. Chem. C, 2003, 118(8), 3764—3774 |
| 25 | Hutchison G. R., Ratner M. A., Marks T. J., J. Am. Chem. Soc., 2005, 127(7), 2339—2350 |
| 26 | Deng W. Q., Goddard W. A., J. Phys. Chem. B, 2004, 108(25), 8614—8621 |
| 27 | Marcus R. A., Rev. Mod. Phys., 1993, 65(3), 599—610 |
| 28 | Zhang S. F., Chen X. K., Fan J. X., Ren A. M., Org. Electron., 2013, 14(2), 607—620 |
| 29 | Schein L. B., Mcghie A. R., Phys. Rev. B, 1979, 20(4), 1631—1639 |
| 30 | Brédas J. L., Beljonne D., Coropceanu V., Cornil J., Chem. Rev., 2004, 104(11), 4971—5004 |
| 31 | Deng W. Q., Sun L., Huang J. D., Chai S., Wen S. H., Han K. L., Nat. Protoc., 2015, 10(4), 632—642 |
| 32 | Rappe A. K., Casewit C. J., Colwell K. S., Goddard W. A. III, Skiff W. M., J. Am. Chem. Soc., 1992, 114(25), 10024—10035 |
| 33 | Maseras F., Morokuma K., J. Comuput. Chem., 1995, 16(9), 1170—1179 |
| 34 | Vreven T., Byun K. S., Komáromi I., Dapprich S., Montgomery John A., Morokuma K., Frisch M. J., J. Chem. Theory Comput., 2006, 2(3), 815 |
| 35 | Chang Y. C., Kuo M. Y., Chen C. P., Lu H. F., Chao I., J. Phys. Chem. C, 2010, 114(26), 11595—11601 |
| 36 | Lin P. P., Zhang S. F., Zhang N. X., Fan J. X., Ji L. F., Guo J. F., Ren A. M., Phys. Chem. Chem. Phys., 2019, 21(6), 3044—3058 |
| 37 | Delgado M. C. R., Kim E. G., Filho D. A. d. S., Bredas J. L., J. Am. Chem. Soc., 2010, 132(10), 3375—3387 |
| 38 | Parker T. M., Burns L. A., Parrish R. M., Ryno A. G., Sherrill C. D., J. Phys. Chem. C, 2014, 140(9), 094106 |
| 39 | Turney J. M., Simmonett A. C., Parrish R. M., Hohenstein E. G., Evangelista F. A., Fermann J. T., Mintz B. J., Burns L. A., Wilke J. J., Abrams M. L., Russ N. J., Leininger M. L., Janssen C. L., Seidl E. T., Allen W. D., Schaefer H. F., King R. A., Valeev E. F., Sherrill C. D., Crawford T. D., Wires. Comput. Mol. Sci., 2012, 2(4), 556—565 |
| [1] | 宋欣, 高申正, 许善磊, 徐浩, 周鑫杰, 朱梦冰, 郝儒林, 朱卫国. 挥发固体添加剂调控有机太阳能电池性能的研究进展[J]. 高等学校化学学报, 2023, 44(9): 20230151. |
| [2] | 陈虹汝, 白阳, 周秋菊, 张志国. 二维核磁在有机光伏中的应用[J]. 高等学校化学学报, 2023, 44(7): 20230104. |
| [3] | 王英杰, 潘泽晖, 陶正煜, 王妍, 童碧海, 冯敏强, 宋明星. 分子间相互作用对苯甲酮类聚集诱导延迟荧光材料性能的影响[J]. 高等学校化学学报, 2023, 44(4): 20220562. |
| [4] | 王剑桥, 马於光. 有机半导体非平衡态HOMO和LUMO能量位移规律与OLED中“热激子”形成的唯象理解[J]. 高等学校化学学报, 2022, 43(4): 20210856. |
| [5] | 林城策, 彭博宇, 李寒莹. 有机单晶电路的研究进展[J]. 高等学校化学学报, 2021, 42(6): 1672. |
| [6] | 马卓远, 汪大洋. 分子自组装单层膜的表面浸润性研究现状和展望[J]. 高等学校化学学报, 2021, 42(4): 1031. |
| [7] | 朱磊, 韩军燕, 常海珍, 邱宇渊, 张雅楠, 彭丹妮, 胡伟, MiaoShaobin. 二胺与二酮环聚合反应的不同途径与产物[J]. 高等学校化学学报, 2018, 39(12): 2686. |
| [8] | 于泳博, 刘翠, 宫利东. 从头算和ABEEMσπ/MM对(CH3OH)n(n=3~12)和[Na(CH3OH)n]+(n=3~6)体系的研究[J]. 高等学校化学学报, 2016, 37(8): 1468. |
| [9] | 陈九菊. 有机半导体Terazulene单晶双极电荷传输性质的理论研究[J]. 高等学校化学学报, 2016, 37(1): 121. |
| [10] | 司朋飞, 罗发亮, 海梅. 聚L-乳酸/4,4'-二羟基二苯硫醚共混物的分子间相互作用及结晶和熔融行为[J]. 高等学校化学学报, 2015, 36(1): 188. |
| [11] | 袁伟, 任清江, 孙恒达, 李慧, 程延祥, 马东阁. 外围取代基团对卟啉铂(Ⅱ)配合物发光性能的影响[J]. 高等学校化学学报, 2014, 35(6): 1229. |
| [12] | 侯海云, 黄银蓉, 白博峰, 杨靖. 293.15 K时咪唑醋酸盐-乙醇二元体系的体积性质及分子间相互作用[J]. 高等学校化学学报, 2014, 35(1): 121. |
| [13] | 孟素慈, 殷秀莲, 马晶, 谢吉民. 有机π共轭配体溶剂化效应与分子间相互作用的理论研究[J]. 高等学校化学学报, 2012, 33(11): 2492. |
| [14] | 梁雪, 孙涛, 王一波. 苯-卤素(X2, X=F, Cl, Br, I)相互作用本质的对称性匹配微扰理论研究[J]. 高等学校化学学报, 2012, 33(03): 541. |
| [15] | 赵建新,乔义涛,冯菁,罗昭峰,袁直 . 共聚物-锌与多肽的相互作用[J]. 高等学校化学学报, 2008, 29(3): 658. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||