联系人简介: 杨玮婷, 女, 博士, 副研究员, 主要从事复合功能多孔材料方面的研究. E-mail: ywt1982@163.com;潘勤鹤, 男, 博士, 教授, 主要从事先进功能材料方面的研究. E-mail: panqinhe@163.com
利用ZnO诱导制备了ZnO@ZIF-8复合微球材料并将其用于溶液中U(Ⅵ) 的去除. 研究表明, 制备的ZnO@ZIF-8复合微球的直径为1~7 μm, pH=4时, 在水溶液中对U(Ⅵ) 的吸附量最大, 达到145.32 mg/g, 吸附机理可能与铀酰离子与复合材料之间的配位作用和氢键作用相关. 考虑到复合微球中用于U(Ⅵ) 吸附的有效成分ZIF-8的含量仅为12.6%, 以ZIF-8含量计算, 该材料对U(Ⅵ) 的单位吸附量高达1137 mg/g.
ZnO@ZIF-8 core@shell microspheres were synthesized by a hydrothermal method and applied for the efficient adsorption of U(Ⅵ) from aqueous solution. The size of synthesized ZnO@ZIF-8 core@shell microspheres was in the range of 1—7 μm. The batch experimental results revealed that the sorption of U(Ⅵ) on ZnO@ZIF-8 was strongly dependent on pH, and the maximum sorption capacity of U(Ⅵ) on ZnO@ZIF-8 was 145.32 mg/g at pH=4.0. The adsorption mechanism could be mainly attributed to the coordination and the hydrogen bonding between ZIF-8 framework and U
当前, 绿色可持续发展已成为推动社会发展的重要方式. 开发高效、 环保的能源以解决全球变暖和化石燃料短缺的问题是实现绿色可持续发展的关键. 核能具有效率高、 无温室气体排放等优点, 作为新型洁净能源已被广泛关注. 近年来, 核能的利用迅速发展, 同时也对人类健康和环境安全造成了极其严重的威胁. 铀是核能的主要核素, 通常以可溶性铀酰离子(U
金属有机框架(MOFs)作为一类经典的多孔材料已被成功用于放射性铀的吸附研究[8, 9, 10, 11, 12, 13, 14, 15]. MOFs由于具有有机-无机杂化的结构类型、 高的比表面积、 可调节的孔径和形状以及可控的功能特性, 使得它们对铀的吸附优于传统的无机多孔材料. 例如Yang等[13]研究了MOF-76在水溶液中对铀的吸附, 铀的平衡吸附量达到298 mg/g, 而且在各种干扰过渡金属离子的存在下, 对U(Ⅵ ) 也具有较好的选择性吸附; Lin等[15]利用Uio-68在水溶液和模拟海水中进行了提取铀的研究, 并通过理论计算分析了官能团与铀酰离子的相互作用; 最近报道的ZIF-67对铀的吸附量已达到了1683.3 mg/g[9]. 氨基、 羧基或胺肟官能团修饰的MIL-101和MIL-53系列不仅对U(Ⅵ ) 表现出了较强的吸附能力, 同时大大提高了吸附选择性[16, 17, 18, 19, 20]. 此外, 与磁性、 光学活性及高分子纤维材料复合的MOFs也被用于溶液中U(Ⅵ ) 的去除和高效选择性分离[21, 22, 23, 24, 25]. 这些结果都表明MOFs及MOFs基复合材料在吸附提取铀元素方面具备了良好的可行性和诱人的前景.
本文利用ZnO诱导制备ZnO@ZIF-8核壳结构的微球材料, 并将其应用于溶液中U(Ⅵ )的去除. 通过扫描电镜(SEM)、 透射电镜(TEM)、 X射线粉末衍射(XRD)、 热重(TG)及元素分析等表征手段研究了制备的ZnO@ZIF-8复合微球的形貌、 结构和组成. 通过U(Ⅵ ) 吸附实验研究了接触时间、 U(Ⅵ ) 浓度、 pH等参数对吸附行为的影响, 为从水溶液中去除放射性核素和减轻环境污染压力提供了一种新材料.
六水合硝酸锌Zn(NO3)2· 6H2O和2-甲基咪唑(C4H6N2)购于阿拉丁试剂有限公司; 乙二胺(C2H8N2)、 甲醇和乙醇购于西陇化工股份有限公司; 六水合硝酸铀酰(UO2)(NO3)2· 6H2O购于湖北楚盛威化工有限公司. 以上试剂均为分析纯.
D8 Advance型X射线粉末衍射仪(德国布鲁克公司, 铜Kα 辐射源, 管电压40 kV, 管电流15 mA, 2θ 扫描范围为5° ~80° , 扫描速度为2° /min); S-4800型扫描电子显微镜(株式会社日立制作所, 加速电压为10 kV); JEM 2100型高分辨透射电子显微镜(日本光学电子公司, 电压200 kV); Q600型热重分析仪(美国TA仪器公司, 在氮气气氛下以10 ℃/min的升温速度程序升温至800 ℃); Vario Micro cube元素分析仪(德国Elementar公司); TU-1901型紫外-可见分光光度计(北京普析通用仪器有限公司).
1.2.1 中空ZnO微球的制备 根据文献[26]方法制备中空ZnO微球: 将0.2 g六水合硝酸锌在搅拌条件下于70 mL乙醇胺溶液中完全溶解, 然后转移至反应釜中, 放入鼓风干燥箱中进行程序升温至180 ℃, 恒温8 h后取出反应釜, 自然冷却至室温. 离心收集固体产物, 用无水乙醇洗涤多次后在60 ℃真空干燥6 h. 将所得氧化锌用研钵研磨成粉状, 然后置于坩埚中, 在马弗炉内以2 ℃/min的速度升温至550 ℃, 煅烧4 h(氧化锌粉末由白色变为灰色), 密封待用.
1.2.2 ZnO@ZIF-8复合微球的制备 将2-甲基咪唑和上述合成的氧化锌微球粉末按照质量比2: 1的比例分别加入到50 mL甲醇中, 搅拌至完全溶解后混合, 并转移至圆底烧瓶中, 于60 ℃恒温反应6 h后离心分离, 并用甲醇洗涤多次以去除未反应的2-甲基咪唑, 收集离心管底部的固体, 于60℃真空干燥6 h, 即得到ZnO@ZIF-8粉末, 密封待用.
将4 mg ZnO@ZIF-8分散于10 mL不同浓度、 不同pH值的U(Ⅵ )水溶液中(用硝酸或氢氧化钠溶液调节铀酰溶液的pH值), 搅拌一定时间后离心分离, 取上层清液稀释, 利用偶氮砷(Ⅲ )法测定剩余溶液中铀的浓度, 通过吸附实验前后溶液中铀浓度变化, 计算ZnO@ZIF-8对铀的吸附量和吸附效率. U(Ⅵ )的吸附量根据公式Qe=(c0-ce)V/m进行计算, 式中: Qe为平衡时ZnO@ZIF-8的吸附量, c0为溶液中U(Ⅵ ) 的初始浓度, ce为溶液中U(Ⅵ ) 的平衡浓度, m为ZnO@ZIF-8微球的质量, V为所配吸附溶液的体积.
1.3.1 pH对铀吸附行为的影响 将4 mg吸附剂加入10 mL U(Ⅵ )浓度为100 mg/L的溶液中, 用硝酸/氢氧化钠调节溶液pH分别为2.0, 3.0, 4.0, 5.0, 6.0, 在室温下磁力搅拌4 h, 吸附完成后进行离心分离, 取适量上层清液检测铀的剩余浓度ce. 根据实验结果得到最佳吸附pH值.
1.3.2 吸附平衡等温线 在pH=4条件下, 取浓度分别为10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 150和200 mg/L的铀溶液10 mL, 加入4 mg吸附剂, 在室温下磁力搅拌4 h. 离心分离, 取适量上层清液用偶氮砷(Ⅲ )法检测溶液中铀的剩余浓度ce, 计算饱和吸附量Qmax.
1.3.3 吸附动力学实验 将4 mg吸附剂加入10 mL U(Ⅵ )浓度为100 mg/L、 pH=4的溶液中, 在室温下磁力搅拌30, 60, 90, 120, 180, 240和300 min后离心分离, 取适量上层清液用偶氮砷(Ⅲ )法检测溶液中铀的剩余浓度ce, 研究吸附动力学.
1.3.4 脱附实验 0.1 mol/L的 Na2CO3 溶液作为洗脱剂. 吸附平衡完成后进行离心分离, 然后用10 mL 洗脱溶液洗脱, 室温下持续搅拌4 h达到平衡, 离心分离后取上层清液用偶氮砷(Ⅲ )法测定铀浓度, 根据脱附前后铀的浓度计算脱附的量和脱附效率(E), E(%)=[(cd-ce)/(c0-ce)]× 100%[式中: c0, ce和cd分别为吸附前、 吸附后和脱附后溶液中U(Ⅵ )的浓度].
1.3.5 溶液中U(Ⅵ )浓度的测定 利用偶氮砷(Ⅲ )法测定铀吸附实验中溶液中剩余U(Ⅵ )含量的具体方法如下: 将吸附后的溶液和偶氮胂(Ⅲ )进行络合, 然后将络合后的溶液稀释10倍, 用硝酸调节溶液pH值为2, 利用紫外分光光度计测定652 nm处的吸光度值, 根据标准曲线求得此时溶液中U(Ⅵ )的平衡浓度. 标准曲线见图S1(见本文支持信息).
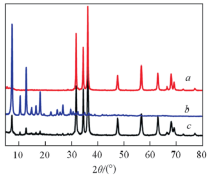
图1为制备的ZnO@ZIF-8的粉末XRD谱图与ZnO和ZIF-8的标准XRD谱图. 可见, 制备的ZnO@ZIF-8复合微球在5° ~20° 之间出现了明显的ZIF-8的峰, 说明ZIF-8成功地复合在最终材料中; 在30° ~80° 之间强的衍射峰与ZnO标准谱图的衍射峰一一对应, 说明合成材料中存在ZnO. 因此, 可以初步判定得到了ZnO和ZIF-8复合的材料.
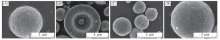
通过SEM观察制备的ZnO和ZnO@ZIF-8微球样品的形貌. 由图2(A)和(B)可以看出, 所得ZnO是微米级球形结构, 表面比较粗糙, 且具有明显的中空结构, 微球的大小为1~7 μ m; 从图2(C)和(D)可以看出生长ZIF-8之后微球尺寸变化不大, 仍然保持很好的分散性, 但ZnO@ZIF-8复合微球表面变得光滑致密, 进一步说明复合微球的表面成功生长了ZIF-8.
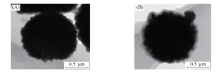
通过TEM分析中空ZnO微球和ZnO@ZIF-8微球样品的形貌和微观结构. 从图3(A)可以看出, ZnO微球表面呈针状, 表面粗糙, 看不到明显的中空结构, 这可能是由于壳层太厚, 电子束无法有效穿透所致; 由图3(B)可以明显地看到微球表面包裹着一层ZIF-8, 表面变得光滑, 这进一步确认了ZnO@ZIF-8微球的核壳结构.
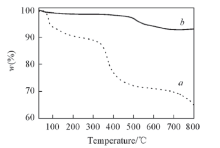
图4为纯ZIF-8和ZnO@ZIF-8的热重曲线. 可见, 纯ZIF-8有2个失重平台, 分别对应300 ℃以前孔道内溶剂分子和表面吸附溶剂的失去以及300 ℃到800 ℃之间ZIF-8骨架的坍塌, 总计失重35.25%. ZnO@ZIF-8复合微球的失重行为则缓和得多, 在500 ℃有一个较明显的失重, 可归结为ZIF-8骨架的坍塌, 总失重率为5.28%. 如果忽略ZnO在此过程中的失重, 则根据该热重结果可计算出ZIF-8在复合材料中的含量为14.9%. ZnO@ZIF-8复合微球的元素分析结果表明, 其碳含量为5.03%, 氮含量为2.54%. 根据元素分析可计算复合材料中ZIF-8含量约为12.6%, 与热重结果基本一致.
2.5.1 溶液pH 对吸附行为的影响 U(Ⅵ )在溶液中的存在形式与浓度和pH密切相关. 对于浓度为100 mg/L的U(Ⅵ )水溶液, 当pH< 4时, 主要以铀酰离子(U
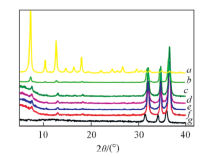 | Fig.5 PXRD patterns of ZIF-8(a), ZnO@ZIF-8(b) and ZnO@ZIF-8 microspheres in aqueous solution with pH of 6(c), 5(d), 4(e), 3(f) and 2(g) |
进一步研究了不同pH值条件下ZnO@ZIF-8复合微球对铀的吸附行为. 由图6可见, 随着溶液的pH值从2逐渐增加到4时, ZnO@ZIF-8复合微球对铀的吸附量显著增加, 在pH=4时吸附量最高, 为145.24 mg/g; 当溶液的pH值进一步增大时, ZnO@ZIF-8对铀的吸附量明显降低, 因此在后续实验中固定溶液的pH值为4.
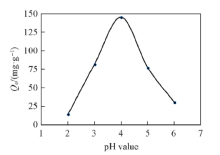 | Fig.6 Effect of pH value of solution on adsorption of uranium by ZnO@ZIF-8 [U(Ⅵ )]initial=100 mg/L, msorbent/Vsolution=0.4 mg/mL, t=4 h. |
2.5.2 吸附动力学 在pH=4的条件下, 研究了吸附剂不同接触时间下对溶液中U(Ⅵ ) 的吸附. 如图7所示, 吸附动力学行为符合拟二阶动力学模型t/Qt=1/(k
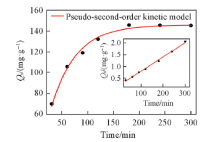 | Fig.7 Effect of reaction time on the uranium adsorption by ZnO@ZIF-8 microspheres [U(Ⅵ )]initial=100 mg/L, msorbent/Vsolution=0.4 mg/mL, pH=4. |
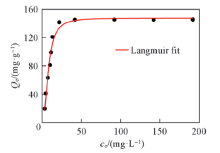
2.5.3 吸附等温线 在pH=4, 吸附时间为4 h的条件下, ZnO@ZIF-8复合微球对水溶液中U(Ⅵ )吸附等温线见图8. 随着溶液初始浓度从10 mg/L增加到80 mg/L时, ZnO@ZIF-8材料对铀的最大吸附量也逐渐增大, 直到80 mg/L时, ZnO@ZIF-8材料对铀的吸附量达到了最大值145.32 mg/g; 随着溶液初始浓度的进一步增大, 铀的最大吸附量不再增加, 图中的曲线趋于平稳. 该吸附行为符合Langmuir模型, 方程为Qe=QmaxKLce/(1+KLce)(其中Qe 为平衡吸附量, Qmax 为最大吸附量, ce为平衡时溶液中U(Ⅵ )的浓度, KL为Langmuir 常数), 根据该式算得最大吸附量Qmax 为147.3 mg/g, 与实际值吻合, KL为0.12 L/mg(R2=0.98). 该吸附等温线表明ZnO@ZIF-8微球材料对铀的吸附主要为单层吸附.
结合图5和图6可知, 在pH=2时ZnO@ZIF-8复合微球表层ZIF-8基本分解了, 主要成分为ZnO, 此时对铀吸附量较低(14.3 mg/g), 说明ZnO对铀吸附作用较弱; 随着溶液pH值增大, 铀吸附量显著增加, 说明对铀吸附起主要作用的组分为复合微球表面的ZIF-8. 我们推测U(Ⅵ ) 与ZIF-8结构的配位作用和氢键作用对吸附起了重要作用[21]. 与已报道的ZIF-8材料(Qmax=523.5 mg/g)相比[21], ZnO@ZIF-8微球的吸附量较低, 这主要因为在该材料中有效吸附组分ZIF-8含量仅为12.6%, 如果仅按有效成分ZIF-8含量进行计算, 其单位吸附量则高达1137 mg/g. 此外, 吸附的铀可通过0.1 mol/L的碳酸钠溶液洗脱, 洗脱率接近85%.
在水热条件下制备了ZnO@ZIF-8核壳结构微球, 该材料的分散性较好, 粒径分布为1~7 μ m. 吸附实验表明该材料在水溶液对U(Ⅵ )的吸附依赖于体系的pH, 在pH=4时, 最大吸附量可达145.32 mg/g, 吸附的机理可能主要跟铀酰离子与复合材料的配位作用和氢键作用有关. 按照有效成分ZIF-8含量计算, 单位吸附量可达1137 mg/g. 本文工件可为进一步研制放射性铀核素的高效吸附材料提供参考.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|